题目内容
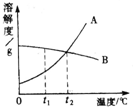
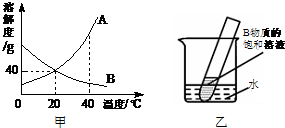 A、B两种物质的溶解度曲线如图甲所示.
A、B两种物质的溶解度曲线如图甲所示.
(1)20℃时,A物质的溶解度为______g.
(2)40℃时,把40g A物质放入100g水中,所得溶液是______(选填“饱和”或“不饱和”)溶液.
(3)20℃时,A物质饱和溶液中溶质的质量分数为______.
(4)如图乙所示,20℃时,将盛有B物质饱和溶液的小试管放入盛水的烧杯中,向水中加入某种物质后,试管中有晶体析出.加入的物质可以是______.
解:(1)20℃时,A物质的溶解度为40g;
(2)观察溶解度曲线图可知:40℃时A的溶解度大于40g,所以把40g A物质放入100g水中可全部溶解依然不饱和;
(3)20℃时A的溶解度是40g,所以A物质饱和溶液中溶质的质量分数为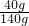 ×100%≈28.6%;
×100%≈28.6%;
(4)由图1可知:B的溶解度随温度的升高而减小;20℃时,将盛有B物质饱和溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出,说明溶液的温度升高,而氢氧化钠固体和氧化钙固体、浓硫酸溶于水均可使溶液的温度升高;
故答案为:(1)40; (2)不饱和; (3)28.6%; (4)氢氧化钠.
分析:(1)根据溶解度曲线可知某温度下物质的溶解度;
(2)根据40℃时A的溶解度分析;
(3)一定温度下,物质的饱和溶液溶质质量分数的计算式是 ×100%,据此分析解答;
×100%,据此分析解答;
(4)B的溶解度随温度的升高而逐渐减小,B物质饱和溶液有晶体析出,说明溶液的温度升高,而氢氧化钠固体和氧化钙固体、浓硫酸溶于水均可使溶液的温度升高.
点评:了解溶解度概念的含义、溶解度曲线的意义、饱和溶液中溶质的质量分数的计算方法、物质溶于水时溶液的温度变化,才能结合题意灵活分析解答.
(2)观察溶解度曲线图可知:40℃时A的溶解度大于40g,所以把40g A物质放入100g水中可全部溶解依然不饱和;
(3)20℃时A的溶解度是40g,所以A物质饱和溶液中溶质的质量分数为
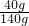 ×100%≈28.6%;
×100%≈28.6%;(4)由图1可知:B的溶解度随温度的升高而减小;20℃时,将盛有B物质饱和溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出,说明溶液的温度升高,而氢氧化钠固体和氧化钙固体、浓硫酸溶于水均可使溶液的温度升高;
故答案为:(1)40; (2)不饱和; (3)28.6%; (4)氢氧化钠.
分析:(1)根据溶解度曲线可知某温度下物质的溶解度;
(2)根据40℃时A的溶解度分析;
(3)一定温度下,物质的饱和溶液溶质质量分数的计算式是
 ×100%,据此分析解答;
×100%,据此分析解答;(4)B的溶解度随温度的升高而逐渐减小,B物质饱和溶液有晶体析出,说明溶液的温度升高,而氢氧化钠固体和氧化钙固体、浓硫酸溶于水均可使溶液的温度升高.
点评:了解溶解度概念的含义、溶解度曲线的意义、饱和溶液中溶质的质量分数的计算方法、物质溶于水时溶液的温度变化,才能结合题意灵活分析解答.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目
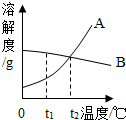 (2004?山西)如图是A、B两种物质的溶解曲线,试回答下列问题:
(2004?山西)如图是A、B两种物质的溶解曲线,试回答下列问题: 如图是A、B两种物质的溶解曲线,试回答下列问题:
如图是A、B两种物质的溶解曲线,试回答下列问题: