题目内容
学习了MnO2对过氧化氢溶液(双氧水)分解有催化作用的知识后,某兴趣小组的同学进行了有关“影响过氧化氢分解速率的因素有哪些”的探究.
【探究一】兴趣小组进行了四个实验,实验数据如表:
(1)通过实验①和②对比可知,过氧化氢分解速率与 有关;实验③和④对比可知,过氧化氢分解速率与温度的关系是 .
(2)用35mL质量分数为30%的双氧水制取氧气,为了减小反应速率,加了一定量的水稀释,这对产生氧气的总质量的影响是 (填“减小”、“不变”或“增大”).
【质疑】CuO能否起到类似MnO2的催化剂作用呢?于是,小组同学又进行了以下探究.
【探究二】
【猜想Ⅰ】CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
【猜想Ⅱ】CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
【猜想Ⅲ】CuO是反应的催化剂,反应前后 .
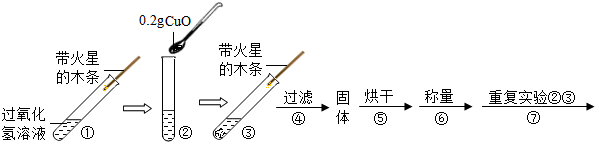
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如图实验:
(1)填写如表:
(2)步骤①的目的是与步骤 作对比,检验加入氧化铜后双氧水的分解速率是否有改变.
(3)步骤④需用到的实验仪器和用品有:铁架台(带铁圈)、漏斗、烧杯、滤纸、 .
(4)过氧化氢能被CuO催化分解放出O2的化学方程式为 .

【探究一】兴趣小组进行了四个实验,实验数据如表:
| 实验 序号 | 过氧化氢的 质量分数/% | 过氧化氢溶液的体积/mL | 温度 /℃ | MnO2的 用量/g | 收集O2的 体积/mL | 反应 时间/s |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| ② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| ③ | 30 | 5 | 35 | 0 | 2 | 49.21 |
| ④ | 30 | 5 | 55 | 0 | 2 | 10.76 |
(2)用35mL质量分数为30%的双氧水制取氧气,为了减小反应速率,加了一定量的水稀释,这对产生氧气的总质量的影响是
【质疑】CuO能否起到类似MnO2的催化剂作用呢?于是,小组同学又进行了以下探究.
【探究二】
【猜想Ⅰ】CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
【猜想Ⅱ】CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
【猜想Ⅲ】CuO是反应的催化剂,反应前后
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如图实验:
(1)填写如表:
| 步骤③的现象 | 步骤⑥的结果 | 步骤⑦的现象 | 结论 |
| 带火星木条 | CuO的质量为 | 带火星木条复燃 | 猜想Ⅰ、Ⅱ不成立;猜想Ⅲ成立 |
(3)步骤④需用到的实验仪器和用品有:铁架台(带铁圈)、漏斗、烧杯、滤纸、
(4)过氧化氢能被CuO催化分解放出O2的化学方程式为
考点:影响化学反应速率的因素探究,催化剂的特点与催化作用,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:【探究一】(1)①②是过氧化氢浓度不同而其他条件相同,这种设计是验证反应物浓度对反应速度的影响;③④则是温度不同其他条件相同,是对温度影响化学反应速度的探究;
(2)根据由于改变的只是溶液的浓度,但是溶质的质量没有改变,所以最终产生的氧气的质量不会改变进行解答;
【猜想Ⅲ】根据催化剂的含义进行解答;
【实验】(1)根据氧化铜对过氧化氢的分解有催化作用回答③现象;根据催化剂的定义和特点回答⑥结果;
(2)根据对比实验的探究方法回答.
(3)根据过滤需要的仪器进行解答;
(4)根据信息结合化学方程式的书写分析.
(2)根据由于改变的只是溶液的浓度,但是溶质的质量没有改变,所以最终产生的氧气的质量不会改变进行解答;
【猜想Ⅲ】根据催化剂的含义进行解答;
【实验】(1)根据氧化铜对过氧化氢的分解有催化作用回答③现象;根据催化剂的定义和特点回答⑥结果;
(2)根据对比实验的探究方法回答.
(3)根据过滤需要的仪器进行解答;
(4)根据信息结合化学方程式的书写分析.
解答:解:【探究一】(1)从表中分析可知:①②是过氧化氢浓度不同而其他的反应时各种量均相同,可知这一过程是考查反应物的浓度与反应速度的关系;则是温度不同其他条件相同,是对温度影响化学反应速度的探究,且温度越高,过氧化氢分解速率越大;
(2)生成物只与反应物量的多少有关,与反应物的浓度无关,反应前后遵循质量守恒定律定律.所以由于改变的只是溶液的浓度,但是溶质的质量没有改变,所以最终产生的氧气的质量不会改变;
【猜想Ⅲ】催化剂的特点是“一变,两不变”,即反应速率变,质量和化学性质不变;
【实验】(1)氧化铜对过氧化氢的分解有催化作用,能加快其分解速率生成氧气的速率,故现象带火星的木条复燃;氧化铜的质量不变,所以为0.2g;
(2)步骤①的目的是与步骤③作对比,检验加入氧化铜后双氧水的分解速率是否有改变;
(3)步骤④需用到的实验仪器和用品有:铁架台(带铁圈)、漏斗、烧杯、滤纸、玻璃棒;
(4)过氧化氢能被CuO催化分解放出O2的化学方程式为2H2O2
2H2O+O2↑.
故答案为:【探究一】
(1)双氧水的浓度(或过氧化氢的质量分数);温度越高,过氧化氢分解速率越大;
(2)不变;
【探究二】质量和化学性质不变;
(1)复燃;0.2;(2)③;(3)玻璃棒;(4)2H2O2
2H2O+O2↑
(2)生成物只与反应物量的多少有关,与反应物的浓度无关,反应前后遵循质量守恒定律定律.所以由于改变的只是溶液的浓度,但是溶质的质量没有改变,所以最终产生的氧气的质量不会改变;
【猜想Ⅲ】催化剂的特点是“一变,两不变”,即反应速率变,质量和化学性质不变;
【实验】(1)氧化铜对过氧化氢的分解有催化作用,能加快其分解速率生成氧气的速率,故现象带火星的木条复燃;氧化铜的质量不变,所以为0.2g;
(2)步骤①的目的是与步骤③作对比,检验加入氧化铜后双氧水的分解速率是否有改变;
(3)步骤④需用到的实验仪器和用品有:铁架台(带铁圈)、漏斗、烧杯、滤纸、玻璃棒;
(4)过氧化氢能被CuO催化分解放出O2的化学方程式为2H2O2
| ||
故答案为:【探究一】
(1)双氧水的浓度(或过氧化氢的质量分数);温度越高,过氧化氢分解速率越大;
(2)不变;
【探究二】质量和化学性质不变;
(1)复燃;0.2;(2)③;(3)玻璃棒;(4)2H2O2
| ||
点评:催化剂、催化作用是初中重要基本概念之一,是考查的重点和热点,主要考查对催化剂、催化作用概念的理解,对催化效率影响因素的探究等.

练习册系列答案
相关题目
下列描述实验现象不正确的是( )
| A、蜡烛在空气里燃烧生成二氧化碳和水 |
| B、氢气在空气里燃烧时产生淡蓝色火焰 |
| C、细铁丝在氧气里点燃剧烈燃烧,火星四射 |
| D、硫在氧气里燃烧发出蓝紫色火焰 |
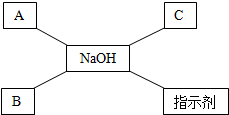 如图是某同学学习了氢氧化钠的化学性质后绘制的知识网络图,其中A、B、C分别表示不同类别的化合物,已知A是一种硫酸盐,其溶液呈蓝色,B能用于灭火,“-”表示相连两物质之间能相互反应.
如图是某同学学习了氢氧化钠的化学性质后绘制的知识网络图,其中A、B、C分别表示不同类别的化合物,已知A是一种硫酸盐,其溶液呈蓝色,B能用于灭火,“-”表示相连两物质之间能相互反应. 某补钙药剂的标签主要内容如图所示,现测定该钙片含量是否符合标注,做如下实验:取10片该钙片,放入干燥、洁净的烧杯中,再向烧杯中加入50g某浓度稀盐酸,恰好完全反应(钙片中其他成分不溶于水,也不和稀盐酸反应,反应中产生的气体全部放出),反应后称量烧杯内剩余物质的质量为64.5g.
某补钙药剂的标签主要内容如图所示,现测定该钙片含量是否符合标注,做如下实验:取10片该钙片,放入干燥、洁净的烧杯中,再向烧杯中加入50g某浓度稀盐酸,恰好完全反应(钙片中其他成分不溶于水,也不和稀盐酸反应,反应中产生的气体全部放出),反应后称量烧杯内剩余物质的质量为64.5g.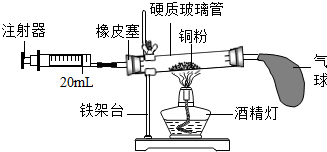 化学实验小组的同学利用下列装置测定空气中氧气的含量.
化学实验小组的同学利用下列装置测定空气中氧气的含量.