题目内容
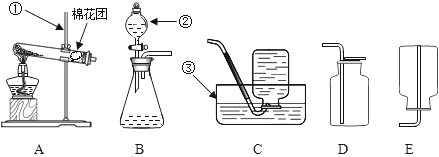
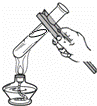
暗紫色固体A在加热的条件下反应生成B和C以及D,常温下过氧化氢溶液遇到C时分解放出D,其中C在反应前后的质量和化学性质都没有改变,若将细铁丝放在D中点燃能剧烈燃烧,火星四射,生成黑色固体E.
(1)写出各物质的名称:
A ; B ;C ; D ;E .
(2)用符号表达式表示有关的化学反应,并指出反应所属的类型(化合反应、分解反应):
① 、( );
② 、( );
③ 、( ).
(3)C是过氧化氢反应中的 .(填“催化剂”或“氧化剂”)
| 物质的鉴别、推断;催化剂的特点与催化作用;反应类型的判定;书写化学方程式、文字表达式、电离方程式.. | |
| 专题: | 常见物质的推断题. |
| 分析: | 根据“常温下过氧化氢溶液遇到C会分解放出D”,且C在反应前后质量和化学性质不变,可推断出C为催化剂;再根据A的颜色为“暗紫色”和“在加热的条件下反应生成B和C以及D”,可推出A;根据细铁丝在D中能剧烈燃烧,可推出D,并知道E,那么也就知道B了. |
| 解答: | 解: (1)根据过氧化氢遇到C时分解放出D,且C反应前后的质量和化学性质不变,可推断出C为二氧化锰,D为氧气;又因为A为暗紫色故A为高锰酸钾,那么B自然是锰酸钾了,细铁丝放在氧气中燃烧生成四氧化三铁,故E自然是四氧化三铁. (2)①高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气.故答案为:2KMnO4 ②实验室用过氧化氢溶液制氧气生成水和氧气.故答案为:2H2O2 ③细铁丝在氧气中燃烧生成四氧化三铁,故答案为:3Fe+2O2 (3)常温下过氧化氢溶液遇到C时分解放出氧气,其中C在反应前后的质量和化学性质都没有改变,故C是二氧化锰,该反应的催化剂. 故答案为: (1)高锰酸钾;锰酸钾;二氧化锰;氧气;四氧化三铁; (2)①2KMnO4 (3)催化剂; |
| 点评: | 解答本题要掌握各种物质的性质方面的知识,只有这样才能对相关方面的问题做出正确的判断. |

下列化学方程式正确的是( )
|
| A. | 2Fe+6HCl═2FeCl3+3H2↑ | B. | 3Fe+2O2═Fe3O4 |
|
| C. | CO+Fe2O3═Fe+2CO2↑ | D. | Fe+CuSO4═Cu+FeSO4 |
空气的净化问题正日益受到人们的关注.下列各组中成分均属于空气污染物的一组是( )
|
| A. | SO2 CO NO2 | B. | CO2 HCl N2 | C. | CH4 CO2 H2 | D. | SO2 N2 O2 |
2006年7月1日,青藏铁路正式通车,许多旅客乘车穿越青藏高原时,会发生高原反应,感到呼吸困难,这是因为高原地区空气里( )
|
| A. | 氧气体积分数大大低于21% |
|
| B. | 氮气体积分数大大超过78% |
|
| C. | 氧气体积分数仍约为21%,但空气稀薄 |
|
| D. | CO2气体含量大大增多 |
近年来,我国多地出现雾霾天气增多现象,下列不属于大气污染物的是( )
|
| A. | 可吸入颗粒物(PM2.5) | B. | CO2 |
|
| C. | NO2 | D. | SO2 |
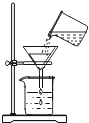
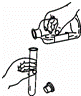
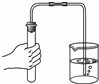
如图所示实验操作正确的是( )
|
| A. |
过滤 | B. |
倾倒液体 | C. |
检查气密性 | D. |
加热液体 |
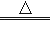 K2MnO4 +MnO2 +O2↑;
K2MnO4 +MnO2 +O2↑;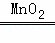 2H2O+O2↑;
2H2O+O2↑; Fe3O4.
Fe3O4.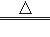 K2MnO4 +MnO2 +O2↑;②2H2O2
K2MnO4 +MnO2 +O2↑;②2H2O2 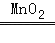 2H2O+O2↑;③3Fe+2O2
2H2O+O2↑;③3Fe+2O2 Fe3O4.
Fe3O4.