题目内容
3.在我国青海湖地区由一种说法:冬天捞碱,夏天晒盐.这里的碱指的是碳酸钠,盐指的是氯化钠.人们从盐湖中捞得的碱会含有少量的氯化钠.某研究性学习小组称取含氯化钠的碳酸钠固体25g,将其配置成100g溶液,再向其中逐滴加入足量的溶质的质量分数为7.3%的稀盐酸,使其恰好完全反应,共收集到8.8g CO2气体.试计算(1)原固体中碳酸钠的质量分数
(2)反应中消耗盐酸的总质量.
(3)最后所得溶液的溶质的质量分数.(计算结果保留到0.1%)
分析 (1)根据二氧化碳的质量和化学方程式可以计算碳酸钠的质量,然后计算碳酸钠的质量分数;
(2)根据二氧化碳的质量求出盐酸溶液中溶质的质量,然后再计算稀盐酸的总质量;
(3)根据题中的数据找出溶质的质量和溶液的质量,然后计算溶质的质量分数.
解答 解:(1)设碳酸钠的质量为x,盐酸溶液中溶质的质量为y,生成氯化钠的质量为z,
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73 117 44
x y z 8.8g
$\frac{106}{x}$=$\frac{73}{y}$=$\frac{117}{z}$=$\frac{44}{8.8g}$
x=21.2g
y=14.6g
z=23.4g
所以原固体中碳酸钠的质量分数为:$\frac{21.2g}{25g}$×100%=84.8%;
反应中消耗盐酸的总质量为:$\frac{14.6g}{7.3%}$=200g;
(3)所以最后所得溶液的溶质的质量分数为:$\frac{23.4g+25g-21.2g}{200g+25g+100g-8.8g}$×100%=8.6%.
故答案为:(1)84.8%;
(2)200g;
(3)8.6%.
点评 根据化学方程式可以表示反应中各物质的质量比,由反应中任意物质的质量可计算出反应中其它物质的质量.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.已知硝酸可发生反应:4HNO3═4NO2↑+X+2H2O.则X的化学式为( )
| A. | NH3 | B. | N2 | C. | O2 | D. | H2 |
11.在点燃条件下,A和B反应生成C和D.反应前后分子种类变化的微观示意图如图:以下说法不正确的是( )
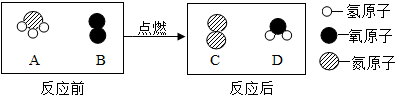

| A. | 这个化学反应共涉及到2种化合物 | |
| B. | 1个A分子中共含有有4个原子 | |
| C. | 在该反应中,生成C和D的质量比为14:27 | |
| D. | 在该反应中,生成C和D的质量比为14:9 |
18.稀盐酸和稀硫酸具有许多相似化学性质的原因是( )
| A. | 它们都是溶液 | B. | 它们都含有酸根离子 | ||
| C. | 它们都含有氢元素 | D. | 它们都电离出了H+ |
8.小明在做过滤操作时,在老师给他的仪器中,他认为还缺少一种,其中老师给的仪器主要有:漏斗、烧杯、滤纸、铁架台(带铁圈),那么他认为缺少的仪器是( )
| A. | 小烧杯 | B. | 长颈漏斗 | C. | 药匙 | D. | 玻璃棒 |
11.下列关于铁的叙述正确的是( )
| A. | 纯铁具有明亮的红色光泽,质硬,延展性好 | |
| B. | 生铁是含杂质较多的铁合金 | |
| C. | 铁器表面涂上油漆的目的只是为了美观 | |
| D. | 铁在潮湿的空气中容易生锈 |