题目内容
实验室要制取氨气,常用氯化铵固体与熟石灰固体混合加热,生成氯化钙,水和氨气,氨气是一种极易溶于水,密度小于空气的具有刺激性气味的气体.氨气能使湿润的酚酞试纸变红色.氨气通过灼热的氧化铜,能使黑色粉末变红色,并有水滴与一种常温下呈气态的单质产生.根据上述信息,回答下列问题:
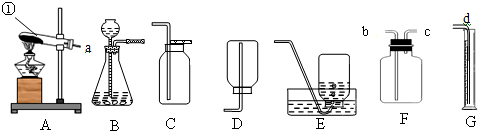
(1)实验室制氨气的发生装置应选用
(2)实验室制氨气的化学方程式为
(3)氨气的水溶液呈
(1)实验室制氨气的发生装置应选用
A
A
(A:氯酸钾制氧气 B:实验室制二氧化碳)的发生装置.氨气的收集方法是向下排空气法
向下排空气法
,理由是氨气易溶于水、密度比空气小
氨气易溶于水、密度比空气小
.(2)实验室制氨气的化学方程式为
2NH4C1+Ca(OH)2═CaCl2+2NH3↑+2H2O
2NH4C1+Ca(OH)2═CaCl2+2NH3↑+2H2O
,氨气与氧化铜反应的化学方程式为2NH3+3CuO
3Cu+N2+3H2O
| ||
2NH3+3CuO
3Cu+N2+3H2O
.
| ||
(3)氨气的水溶液呈
碱
碱
(酸、中、碱)性,氨气具有还原性
还原性
(氧化性,还原性)分析:(1)制取氨气的发生装置由反应物的状态和反应条件决定;收集装置主要由气体的密度和溶水性决定;可以据此解答该题.
(2)根据氨气的制取及氨气与氧化铜的反应写出反应的方程式;
(3)根据氨气的性质分析回答.
(2)根据氨气的制取及氨气与氧化铜的反应写出反应的方程式;
(3)根据氨气的性质分析回答.
解答:解:(1)实验室常用氯化铵固体和熟石灰固体混合加热来制取氨气;该反应中反应物的状态是固态,反应条件是加热,所以应选固固加热型的发生装置,即应该选择用氯酸钾制氧气的装置;由于氨气易溶于水、密度比空气小,可用向下排空气法收集.
(2)由题意可知,实验室要制取氨气,常用氯化铵固体与熟石灰固体混合加热,生成氯化钙,水和氨气.反应的方程式:2NH4C1+Ca(OH)2═CaCl2+2NH3↑+2H2O.由于氨气通过灼热的氧化铜,能使黑色粉末变红色,并有水滴与一种常温下呈气态的单质产生.由质量守恒定律可知,气态单质是氮气.所以,反应的方程式是:2NH3+3CuO
3Cu+N2+3H2O.
(3)由题意可知,氨气能使湿润的酚酞试纸变红色,说明氨气的水溶液呈碱性;由于氨气能将氧化铜还原成铜,说明了氨气具有还原性.
故答为:(1)A;向下排空气法;氨气易溶于水、密度比空气小.(2)2NH4C1+Ca(OH)2═CaCl2+2NH3↑+2H2O;2NH3+3CuO
3Cu+N2+3H2O.(3)碱;还原性.
(2)由题意可知,实验室要制取氨气,常用氯化铵固体与熟石灰固体混合加热,生成氯化钙,水和氨气.反应的方程式:2NH4C1+Ca(OH)2═CaCl2+2NH3↑+2H2O.由于氨气通过灼热的氧化铜,能使黑色粉末变红色,并有水滴与一种常温下呈气态的单质产生.由质量守恒定律可知,气态单质是氮气.所以,反应的方程式是:2NH3+3CuO
| ||
(3)由题意可知,氨气能使湿润的酚酞试纸变红色,说明氨气的水溶液呈碱性;由于氨气能将氧化铜还原成铜,说明了氨气具有还原性.
故答为:(1)A;向下排空气法;氨气易溶于水、密度比空气小.(2)2NH4C1+Ca(OH)2═CaCl2+2NH3↑+2H2O;2NH3+3CuO
| ||
点评:熟悉实验室制取氢气、氧气、二氧化碳的发生装置和收集装置,能写出各反应的反应原理是解答此题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
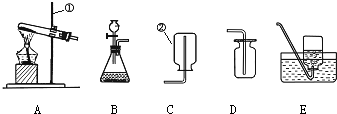
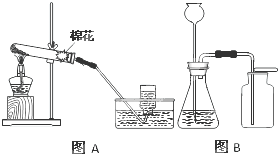 实验室常里用于制取氧气的方法有:a、加热氯酸钾晶体和二氧化锰粉末;
实验室常里用于制取氧气的方法有:a、加热氯酸钾晶体和二氧化锰粉末;