题目内容
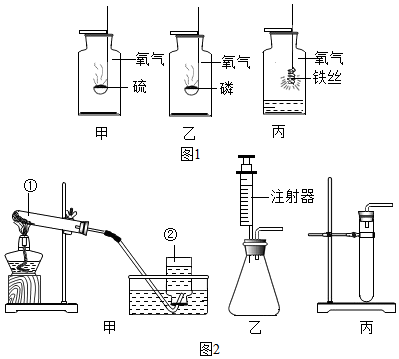
16. 小刚和小丽两位同学用如图所示装置进行实验,验证二氧化碳能和氢氧化钠发生反应.
小刚和小丽两位同学用如图所示装置进行实验,验证二氧化碳能和氢氧化钠发生反应.(1)小刚关闭K,通入二氧化碳,A、B中均无明显变化.则B中盛放氢氧化钙溶液.
(2)小刚打开K,继续通入二氧化碳.B中反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O此步实验的目的是验证二氧化碳与氢氧化钙能发生反应.
(3)小丽认为:通常状态下,1体积的水约能溶解1体积的二氧化碳,因此上述实验不足证明二氧化碳和氢氧化钠发生了反应.于是小丽用洗涤干净的上述装置重新试验,分别量取50mL上述溶液放入A、B中,关闭K,通入约500mL二氧化碳,A、B中均无明显变化.此实验可以说明二氧化碳和氢氧化钠发生了反应,其理由是关闭K时,B中溶液无明显变化,且通入的二氧化碳体积远大于A中溶液的体积,说明二氧化碳和氢氧化钠发生了反应.
分析 (1)小刚关闭K,通入二氧化碳,A、B中均无明显变化.可推测B中盛放的物质,假设A中为氢氧化钙,则一定变浑浊;
(2)小刚关闭K,继续通入二氧化碳,A中氢氧化钠溶液反应完,所以二氧化碳与B中物质反应;
(3)已知“通常状况下,1体积的水约能溶解1体积二氧化碳”,则量取50ml上述溶液放入A,最多溶解50ml二氧化碳,剩余的二氧化碳一定与氢氧化钠溶液反应,否则B不会无明显变化.
解答 解:(1)小刚关闭K,通入二氧化碳,A、B中均无明显变化.假设A中为氢氧化钙,则一定变浑浊;可推测B中盛放的物质为氢氧化钙,无现象,因为二氧化碳被氢氧化钠溶液吸收干净;
(2)小刚关闭K,继续通入二氧化碳,A中氢氧化钠溶液反应完,所以二氧化碳与B中氢氧化钙溶液,故化学方程式为:
Ca(OH)2+CO2=CaCO3↓+H2O;此步实验目的是验证二氧化碳与氢氧化钙能发生反应;
(3)已知“通常状况下,1体积的水约能溶解1体积二氧化碳”,则量取50ml上述溶液放入A,最多溶解50ml二氧化碳,剩余的二氧化碳一定与氢氧化钠溶液反应,而剩余的二氧化碳再与氢氧化钙反应,所以“A、B中均无明显变化”.故小丽用洗涤干净的上述装置重新实验,分别量取50ml上述溶液放入A、B中,关闭K,通入约500ml二氧化碳,A、B中均无明显变化.此实验可以说明二氧化碳和氢氧化钠发生了反应,其理由是关闭K时,B中溶液无明显变化,且通入的二氧化碳体积远大于A中溶液的体积,说明二氧化碳和氢氧化钠发生了反应.
故答为:(1)氢氧化钙;(2)Ca(OH)2+CO2=CaCO3↓+H2O;验证二氧化碳与氢氧化钙能发生反应;
(3)关闭K时,B中溶液无明显变化,且通入的二氧化碳体积远大于A中溶液的体积,说明二氧化碳和氢氧化钠发生了反应.
点评 掌握探究二氧化碳性质的方法与技巧;了解反应现象和本质的联系,学会根据现象总结反应结论.

| A. | 3H--3个氢分子 | B. | 2H2O--2个水分子 | C. | 硫酸钾--KSO4 | D. | 氧化镁--Mg2O2 |
【实验装置】
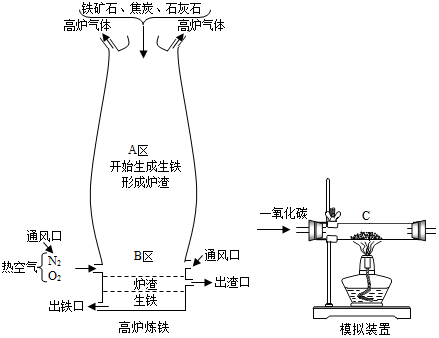
写出A区和B区所发生反应的主要方程式:
A区Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;B区C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2、CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
【提出问题】
观察黑色粉末有两种,黑色粉末成分是什么呢?
【查阅资料】
| 物质 | 四氧化三铁 | 氧化亚铁 | 铁粉 |
| 颜色 | 黑色 | 黑色 | 黑色 |
| 能否被磁铁吸引 | 能 | 不能 | 能 |
| 与盐酸反应溶液颜色 | 黄色 | 浅绿色 | 浅绿色 |
【假设猜想】
猜想①:含有铁、氧化亚铁. 猜想②:含有铁、四氧化三铁. 猜想③:含有铁、氧化亚铁和四氧化三铁.
【实验方案】请写出实验操作,与表中结论相符的预期现象.
| 实验方法 | 实验操作 | 预期现象 | 结论 |
| 物理方法 | 步骤1 | 黑色粉末全部被吸引 | 猜想②成立 |
| 化学方法 | 步骤2 | 产生气泡,溶液变成黄色 |
(1)生铁口低于出渣口的原因生铁的密度大于炉渣的密度;
(2)在做模拟实验中发现其存在一个很不环保的缺陷,如何进缺陷:尾气没有处理;
处理尾气的方法:点燃尾气,或利用塑料袋收集尾气.

 目前,随着国际市场石油价格的不断攀升,能源问题受到了全世界的关注.如图是2004年我国化石燃料可供使用的年限统计示意图,该图告诉了我们什么?我们应该怎么做(写出两点)?
目前,随着国际市场石油价格的不断攀升,能源问题受到了全世界的关注.如图是2004年我国化石燃料可供使用的年限统计示意图,该图告诉了我们什么?我们应该怎么做(写出两点)?