题目内容
8.味精是常用的调味品,它的鲜味来自于其中的主要成分谷氨酸钠化学式为C5H8NO4Na,请回答下列问题(1)钠的相对分子质量为23,其中碳、氧元素的质量比是15:16.
(2)味精中还含有NaCl(其他成分不考虑).某兴趣小组为测定某品牌味精中NaCl的质量分数,进行了如下实验:将5g味精溶于足量水中,向其中加入过量的AgNO3溶液(反应的方程式为NaCl+AgNO3═NaNO3+AgCl↓)得到AgCl白色沉淀2.87g,请计算所用品牌味精中NaCl的质量分数.
分析 (1)根据钠的相对原子质量和谷氨酸钠化学式计算回答;
(2)根据氯化钠与硝酸银反应的方程式,由AgCl白色沉淀的质量可就出氯化钠的质量.即可求出所用品牌味精中NaCl的质量分数.
解答 解:(1)钠的相对分子质量为23,谷氨酸钠中碳、氧元素的质量比是:(12×5):(16×4)=15:16;
(2)设氯化钠的质量为x
NaCl+AgNO3═NaNO3+AgCl↓
58.5 143.5
x 2.87g
$\frac{58.5}{143.7}=\frac{x}{2.87g}$ 解得:x=1.17g
所用品牌味精中NaCl的质量分数是:$\frac{1.17g}{5g}×100%$=23.4%.
故答为:(1)23,15:16;(2)所用品牌味精中NaCl的质量分数是23.4%.
点评 本题主要考查了根据化学式、方程式的计算,难度不大,属于基础的计算,注意计算的数据要准确.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
18.下列有关物质的用途正确的是( )
| A. |  车灯内充入氮气能发出不同颜色的光 | |
| B. |  利用液氧冷冻麻醉做手术 | |
| C. |  焊接金属时氢气作保护气 | |
| D. |  神舟十一号中宇航员利用携带的空气呼吸 |
16.在我们的日常生活中设计许多变化,下列过程一定包含化学变化的是( )
| A. | 森林火灾 | B. | 山体滑坡 | C. | 棉线织布 | D. | 冰块制成冰雕 |
18.化学是一门以实验为基础的科学,在如图所示的实验操作中正确的是( )
| A. | 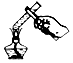 加热液体 | B. | 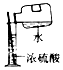 稀释浓硫酸 | ||
| C. | 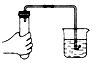 检査装置的气密性 | D. | 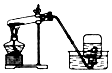 高锰酸押制取氧气 |
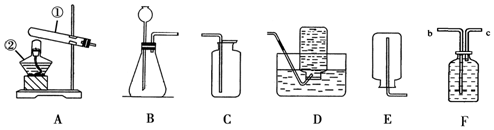
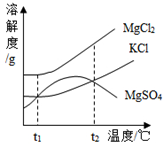 利用卤水晒盐后得到的晶体是粗盐,剩余的液体称为苦卤,苦卤中除氯化钠外还含有多种成分,在食品、化工等方面有重要应用.请根据已知信息回答下列问题.
利用卤水晒盐后得到的晶体是粗盐,剩余的液体称为苦卤,苦卤中除氯化钠外还含有多种成分,在食品、化工等方面有重要应用.请根据已知信息回答下列问题.