题目内容
(7分)(1)学校运动会上短跑项目“发令枪”里的火药成分为KClO3、MnO2和红磷,当扣动扳机时,①撞针撞击火药,产生热量使KClO3分解产生O2 ②并引燃红磷产生白烟.试写出①中发生反应的化学方程式_________;②中发生的反应属于基本反应类型中的_______。
(2)“84”消毒液可用于灾区防疫,其主要成分是次氯酸钠(NaClO),制取它的化学方程式为2NaOH+X═NaClO+NaCl+H2O,则X的化学式为___________.求出NaClO中氯元素化合价并在该化学式中表示出来___________________。
(3)固体MgH2是氢能源汽车的供能剂,MgH2可以和水反应生成一种氢氧化物,同时释放出氢气,该反应的化学方程式是___________________________________。
(1)①2KClO3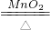 2KCl+3O2↑ 化合反应
2KCl+3O2↑ 化合反应
(2)Cl2 NaClO (3)MgH2+2H2O=Mg(OH)2+2H2↑
【解析】
试题分析:(1)①①撞针撞击火药,产生热量使KClO3分解产生O2,发生反应的化学方程式:2KClO3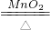 2KCl+3O2↑;②中发生的反应:4P + 5O2 点燃 2P2O5,属于基本反应类型中的化合反应
2KCl+3O2↑;②中发生的反应:4P + 5O2 点燃 2P2O5,属于基本反应类型中的化合反应
(2)根据质量守恒定律的微观解释:在化学反应前后,原子的种类、个数都不变,结合化学反应:2NaOH+X═NaClO+NaCl+H2O,则X的化学式为Cl2;化合价的表示方法:在元素符号正上方标出化合价。符号在前,数字在后。若数字为1时,不能省略,故NaClO中氯元素化合价:NaClO
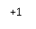 (3)MgH2可以和水反应生成一种氢氧化物,同时释放出氢气,根据质量守恒定律,可推断一种氢氧化物应为Mg(OH)2,故该反应的化学方程式是:MgH2+2H2O=Mg(OH)2+2H2↑
(3)MgH2可以和水反应生成一种氢氧化物,同时释放出氢气,根据质量守恒定律,可推断一种氢氧化物应为Mg(OH)2,故该反应的化学方程式是:MgH2+2H2O=Mg(OH)2+2H2↑
考点:化学方程式的书写,质量守恒定律,基本反应类型,化合价的表示方法

 阅读快车系列答案
阅读快车系列答案(10分)某化学兴趣小组回收利用废旧干电池。
实验1:回收填料中的二氧化锰和氯化铵
查阅资料:废旧干电池填料的主要成分为二氧化锰、炭粉、氯化铵和氯化锌等,其中氯化铵、氯化锌可溶于水。兴趣小组的同学们设计回收物质的流程如图所示。
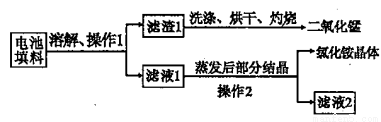
(1)操作1和操作2的名称都是_______,该操作中玻璃棒的作用是_______________。
(2)灼烧滤渣l的目的是________________________ 。
实验2:利用外壳回收物锌制取氢气及相关探究
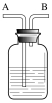
(3)用锌和稀硫酸制取氢气。己知氢气密度比空气小且难溶于水,提供装置如图。
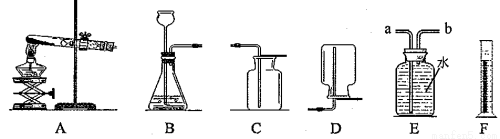
①应选择的制取和收集装置为______(填编号)。
②若用排水法收集并测定气体的体积,则应选用的装置为________。
(4)探究影响锌与稀硫酸反应快慢的因素。反应过程中,用前10min内收集的氢气体积来比较反应的快慢。控制其他条件相同,进行下表三组实验,获得数据如下表。
实验编号 | 试剂 | 前 10 min 内产生的氢气体积(mL) | |
不同纯度的锌 | 不同浓度的稀硫酸 | ||
a | 纯锌 | 30 mL 30 % | 564.3 |
b | 含杂质的锌 | 30 mL 30 % | 634.7 |
c | 纯锌 | 30 mL 20 % | 449.3 |
①比较实验 a 和实验 b ,可以得到的结论是________________________。
②为了研究硫酸浓度对反应快慢的影响,需比较实验__________(填编号)。
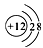 ,表示的是一种金属原子
,表示的是一种金属原子