题目内容
2.通过海水晒制可得粗盐,粗盐中除NaCl外,还含有MgCl2、CaCl2、MgSO4以及泥沙等杂质.以下是一种由粗盐制备精盐的实验方案流程图:
分析该流程图,回答下列问题:
(1)试剂X为Na2CO3(填写化学式).
(2)试剂Y为HCl.(填写化学式).
(3)操作Z为蒸发结晶.
(4)选择的除杂的试剂不能用KOH代替NaOH溶液,理由是会引入新杂质KCl.
分析 粗盐中的MgCl2、CaCl2、Na2SO4都溶于水,要想将杂质除去必须将MgCl2、CaCl2和Na2SO4转化为沉淀,连同泥沙一起过滤除去.
解答 解:本实验的过程为;①粗盐提纯的第一步是溶解,搅拌时要用到玻璃棒,以加快粗盐溶解.
②加入过量BaCl2溶液,与Na2SO4发生反应,生成BaSO4沉淀和NaCl;
③加过量NaOH溶液,与MgCl2发生反应,生成Mg(OH)2沉淀和氯化钠;
④加过量Na2CO3溶液,与CaCl2和①中过量BaCl2溶液发生反应,生成CaCO3沉淀和BaCO3沉淀和氯化钠;
⑤过滤,滤出前面生成的沉淀及泥沙;
⑥加适量盐酸,与③中过量NaOH溶液和②中过量Na2CO3溶液发生反应,生成氯化钠、水和二氧化碳气体.
⑦氯化钠溶液蒸发、结晶,得到精盐.
故答案为:
(1)Na2CO3
(2)HCl
(3)蒸发结晶
(4)会引入新杂质KCl
点评 本题主要考查了粗盐提纯过程中的除杂方面的知识,综合性强,双基要求高.

练习册系列答案
相关题目
12.环保部门测定某雨水中含有亚硫酸(H2SO3),雨水的pH变化如下表所示.已知该酸不稳定,且比硫酸酸性弱,在空气中易发生反应:2H2SO3+O2=2H2SO4.下列说法不正确的是( )
| 测定时间/分钟 | 1 | 2 | 3 | 4 | 5 |
| pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
| A. | 酸雨可腐蚀某些金属制品 | |
| B. | 雨水酸性逐渐减弱 | |
| C. | 主要是因为雨水中的成分发生变化,溶液pH发生变化 | |
| D. | 酸雨主要是因为空气受到SO2及氮氧化物的污染形成的 |
11.已知某固体粉末由氯化钾、硝酸钡、硫酸亚铁、硫酸钠、碳酸钠、硝酸镁中的一种或几种组成.取少量该粉末加入足量水,振荡后得白色浑浊液,再加足量稀盐酸,沉淀不溶解,过滤得白色沉淀X和无色溶液Y,向Y中滴加硝酸银溶液,又产生白色沉淀Z.下列结论错误的是( )
| A. | 原固体粉末含有Ba(NO3)2、Na2SO4、KCl | |
| B. | X、Z分别是BaSO4和AgCl | |
| C. | 原粉末一定不含FeSO4和Na2CO3 | |
| D. | 无法确定原粉末中是否含有Mg(NO3)2 |
12.比较推理是化学学习中常用的思维方法,下列有关比较推理中正确的是( )
| A. | 单质中只有一种元素,所以只有一种元素的物质一定是单质 | |
| B. | 中和反应一定有盐和水生成,所以有盐和水生成的反应一定是中和反应 | |
| C. | 铁和铜都是金属,铁与稀硫酸反应产生氢气,则铜也能与稀硫酸反应产生氢气 | |
| D. | H20和H2O2分子构成不同,所以化学性质不同 |
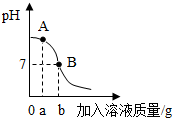 如图是稀HCl和NaOH溶液反应的pH变化曲线图,从图中可以看出该实验中是将稀盐酸滴入氢氧化钠溶液;当加入溶液质量是ag时,此时混合溶液中溶质为氯化钠和氢氧化钠;反应的化学方程式是NaOH+HCl=NaCl+H2O.
如图是稀HCl和NaOH溶液反应的pH变化曲线图,从图中可以看出该实验中是将稀盐酸滴入氢氧化钠溶液;当加入溶液质量是ag时,此时混合溶液中溶质为氯化钠和氢氧化钠;反应的化学方程式是NaOH+HCl=NaCl+H2O.