题目内容
1.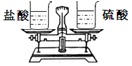 在天平的两端左右各放一杯质量和质量分数都相等的盐酸和硫酸溶液,天平平衡,现在两边各加入质量相等的镁条,如图所示,充分反应后,请问下列说法正确的是( )
在天平的两端左右各放一杯质量和质量分数都相等的盐酸和硫酸溶液,天平平衡,现在两边各加入质量相等的镁条,如图所示,充分反应后,请问下列说法正确的是( )| A. | 反应结束后,如果只有一杯里的金属有剩余,则一定是左盘有剩余 | |
| B. | 反应结束后,如果两边的金属都反应完全,则往右盘里滴加碳 酸钠一定会有气泡产生 | |
| C. | 反应结束后,如果两边的金属都有剩余,则天平继续保持平衡 | |
| D. | 以上三种说法都不对 |
分析 根据镁和盐酸反应生成氯化镁和氢气,镁和硫酸反应生成硫酸镁和氢气,依据选项中假设的情况进行具体的分析.
解答 解:在天平的两端左右各放一杯质量和质量分数都相等的盐酸和硫酸溶液,天平平衡,可以假设参加反应的酸的质量都是98
Mg+2HCl═MgCl2+H2↑
24 73 2
32.2 98 2.7
Mg+H2SO4═MgSO4+H2↑
24 98 2
24 98 2
A、通过化学方程式可以看出,与相同质量的酸反应时,右边镁消耗的少,所以反应结束后,如果只有一杯里的金属有剩余,则一定是右盘有剩余,故A错误;
B、通过化学方程式可以看出,与相同质量的金属反应时,硫酸消耗的多,所以反应结束后,如果两边的金属都反应完全,盐酸一定有剩余,则往左盘里滴加碳酸钠一定会有气泡产生,故B错误;
C、反应结束后,如果两边的金属都有剩余,酸完全反应,但是等质量的盐酸和硫酸中含有的氢元素质量不相等,依据质量守恒定律可知,生成的氢气质量也不会相等,所以天平不能继续保持平衡,故C错误;
D、以上三种说法都不对,故D正确.
故选:D.
点评 本题考查了金属与酸反应生成氢气质量的关系,完成此题,可以依据反应的化学方程式,从酸的质量和金属的质量的角度进行解答.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
11.下列说法中,正确的是( )
| A. | 食品包装中充入氮气以防腐 | |
| B. | 新鲜空气中不含二氧化碳 | |
| C. | 空气中的氮气、氧气不再保持各自的化学性质 | |
| D. | 磷在空气中燃烧,反应剧烈,产生大量白雾 |
12.如表有关物质的检验、区分、分离、提纯所用的试剂或方法错误的是( )
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 检验NH4NO3溶液和K2SO4溶液 | NaOH溶液或Ba(NO3)2溶液 |
| B | 除去生石灰中含有的杂质石灰石 | 水或稀盐酸 |
| C | 从H2O2溶液制氧气的残余物中分离出MnO2 | 过滤或蒸发 |
| D | 区分失去标签的浓硫酸和稀硫酸 | 水或餐巾纸 |
| A. | A | B. | B | C. | C | D. | D |
9.科学家发明了一种车用制氢装置,其制取氢气的原理:硼(B)和水在高温下反应生成氢氧化硼和氢气.该反应的化学方程式为:2B+6H2O$\frac{\underline{\;高温\;}}{\;}$2B(OH)3+3H2,则这个反应属于( )
| A. | 分解反应 | B. | 化合反应 | C. | 置换反应 | D. | 复分解反应 |
6.李老师乘高铁去杭州听课,从安全角度考虑,以下四种物质中,允许旅客带上高铁的是( )
| A. | 浓硫酸 | B. | 食盐 | C. | 酒精 | D. | 白磷 |
10. 如图是某广口瓶的标签,已经部分被污损和腐蚀.小明想探究其成分,他取一支洁净的试管,加入少量广口瓶中的固体,滴入少量盐酸,有无色无味气泡产生.该气体能使澄清石灰水变浑浊,则该固体( )
如图是某广口瓶的标签,已经部分被污损和腐蚀.小明想探究其成分,他取一支洁净的试管,加入少量广口瓶中的固体,滴入少量盐酸,有无色无味气泡产生.该气体能使澄清石灰水变浑浊,则该固体( )
 如图是某广口瓶的标签,已经部分被污损和腐蚀.小明想探究其成分,他取一支洁净的试管,加入少量广口瓶中的固体,滴入少量盐酸,有无色无味气泡产生.该气体能使澄清石灰水变浑浊,则该固体( )
如图是某广口瓶的标签,已经部分被污损和腐蚀.小明想探究其成分,他取一支洁净的试管,加入少量广口瓶中的固体,滴入少量盐酸,有无色无味气泡产生.该气体能使澄清石灰水变浑浊,则该固体( )| A. | 一定是Na2CO3 | B. | 可能是Na2CO3,也可能是NaHCO3 | ||
| C. | 一定是NaHCO3 | D. | 一定是Na2CO3和NaHCO3的混合物 |
11.2013年我国许多地区雾霾天气频发,造成雾霾的一个因素是机动车排放的尾气.而“催化转化器”可以将汽车尾气中有害气体处理为无污染的气体,下图为该反应的微观示意图,其中不同颜色的球代表不同的原子.下列说法错误的是( )
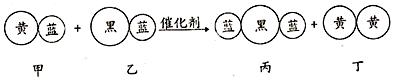

| A. | 该反应中共有三种元素 | B. | 乙和丙中所含的元素种类相同 | ||
| C. | 乙和丙都是化合物 | D. | 甲和丁中同种元素的化合价相等 |
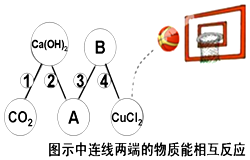 物质王国举行一场趣味篮球赛.某队由CO2、Ca(OH)2、CuCl2、HCl、Fe五名“队员”组成,队员只能将球传递给可以与自己发生化学反应的队员.比赛中,由CO2“队员”先发球,
物质王国举行一场趣味篮球赛.某队由CO2、Ca(OH)2、CuCl2、HCl、Fe五名“队员”组成,队员只能将球传递给可以与自己发生化学反应的队员.比赛中,由CO2“队员”先发球,