题目内容
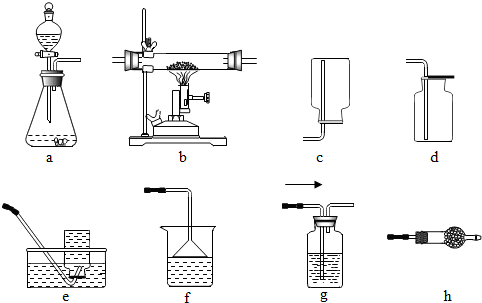
 如图所示,天平处于平衡状态.现向左右两杯溶液中加入等质量的两块铁片,过一会取出,此时天平( )
如图所示,天平处于平衡状态.现向左右两杯溶液中加入等质量的两块铁片,过一会取出,此时天平( )| A、仍将平衡 |
| B、左升,右降 |
| C、左降,右升 |
| D、以上都有可能 |
考点:金属的化学性质
专题:金属与金属材料
分析:根据金属活动性顺序及各物质发生化学反应时的质量关系来分析作答.在金属活动性顺序表中,氢前面的金属能和常见的酸反生置换反应,位于前面的金属能把排在它后面的金属从其盐溶液中转换出来.
解答:解:把铁片放入CuSO4溶液中,铁能把铜置换出来,铜附着在铁片上;根据化学方程式,利用差量法:
Fe+CuSO4═FeSO4+Cu…△m.
56 64 …8
则可知固体质量增加8g,溶液质量减少8g.
把铁片放入稀硫酸溶液中,铁片能和稀硫酸反应生成可溶于水的硫酸亚铁和氢气,氢气逸出,根据化学方程式,利用差量法:
Fe+H2SO4═FeSO4+H2↑…△m.
56 2 …54
则可知固体质量减少56g,生成氢气2g,溶液质量增加了54g.
根据题意“两块铁片,过一会取出”,故可知左边溶液质量减小,右边溶液质量增大.
故选:B.
Fe+CuSO4═FeSO4+Cu…△m.
56 64 …8
则可知固体质量增加8g,溶液质量减少8g.
把铁片放入稀硫酸溶液中,铁片能和稀硫酸反应生成可溶于水的硫酸亚铁和氢气,氢气逸出,根据化学方程式,利用差量法:
Fe+H2SO4═FeSO4+H2↑…△m.
56 2 …54
则可知固体质量减少56g,生成氢气2g,溶液质量增加了54g.
根据题意“两块铁片,过一会取出”,故可知左边溶液质量减小,右边溶液质量增大.
故选:B.
点评:解答本题时要求学生能掌握常见金属的活动性顺序表及其应用,并且根据能发生反应的各物质之间的质量比来对选项进行分析.

练习册系列答案
相关题目
下列对分子、原子、离子的说法中,错误的是( )
| A、相同原子可以构成不同分子 |
| B、任何离子内质子数和核外电子数肯定不相等 |
| C、原子能构成分子,但不能直接构成物质 |
| D、化学变化的实质是分子分裂成原子,原子重新组合成新分子 |
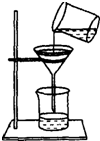 程伟同学将浑浊的湖水样品,倒入烧杯中,先加人明矾粉末搅拌溶解,静置一会儿后,采用下列装置进行过滤,请问:
程伟同学将浑浊的湖水样品,倒入烧杯中,先加人明矾粉末搅拌溶解,静置一会儿后,采用下列装置进行过滤,请问: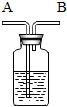 归纳总结、分类是化学学习的一种重要方法,下题中先在A、B、C中选择一个正确选项,将正确选项的代号填涂在答题卷的相应位置上,然后在D处补充一个符合题意的答案.
归纳总结、分类是化学学习的一种重要方法,下题中先在A、B、C中选择一个正确选项,将正确选项的代号填涂在答题卷的相应位置上,然后在D处补充一个符合题意的答案.