题目内容
维生素C是生命活动中不可缺少的营养物质,不同的饮料中维生素C的含量不同。下面是
小明同学运用学到的实验方法测定橙汁、果味饮料中维生素C的含量。 [实验目的] 测定不同饮料中维生素C的含量。
[实验目的] 测定不同饮料中维生素C的含量。 [实验原理](1)维生素C是一种无色易溶于水的有机物,能与碘水反应,使碘水褪色;
[实验原理](1)维生素C是一种无色易溶于水的有机物,能与碘水反应,使碘水褪色; (2)淀粉遇
(2)淀粉遇 到碘水变 色。
到碘水变 色。 [实验试剂] 碘水、淀粉溶液、已知浓度的标准维生素C溶液、蒸馏水
[实验试剂] 碘水、淀粉溶液、已知浓度的标准维生素C溶液、蒸馏水 [实验过程]
[实验过程] 步骤1:在4支试管中分别盛有3.0 mL的下列物质:①蒸馏水,②标准维生素C溶液,
步骤1:在4支试管中分别盛有3.0 mL的下列物质:①蒸馏水,②标准维生素C溶液, ③橙汁,④果味饮料。分别向4支试管中滴加2滴淀粉溶液。
③橙汁,④果味饮料。分别向4支试管中滴加2滴淀粉溶液。 步骤2:用4支相同的胶头滴管分别向①~④支试管中逐滴滴加碘水至刚好变色,并记录滴数。
步骤2:用4支相同的胶头滴管分别向①~④支试管中逐滴滴加碘水至刚好变色,并记录滴数。 [实验记录]
[实验记录]
| 测定物质 | ① | ② | ③ | ④ |
| 滴入碘水的数量(滴) | 1 | 8 | 15 | 5 |
试回答下列问题: (1)你认为小明测定的两种饮料中, 的维生素C的含量较高。
(1)你认为小明测定的两种饮料中, 的维生素C的含量较高。 (2)有的同学认为测定物质标准维生素C溶液是多余的,你认为呢?请说明理由:
(2)有的同学认为测定物质标准维生素C溶液是多余的,你认为呢?请说明理由:
。(3)化学实验需要控制变量。下列 (填序号)情况会影响到测定结果。
A.每次实验所用饮料的颜色不同 B.量取的被测试物质的体积不同 C.试管的大小不同 D.没有
C.试管的大小不同 D.没有 用同一规格的胶头滴管滴加碘水
用同一规格的胶头滴管滴加碘水 [回顾与反思] 实验中所用的淀粉溶液的作用是 。
[回顾与反思] 实验中所用的淀粉溶液的作用是 。
饮料中维生素C的浓度(其他合理答案也可)
(3)A、B、D
[回顾与反思] 确定维生素C是否与碘水完全反应
【解析】根据[实验记录]滴加碘水的滴数越多,该饮料中含有的维生素C越多,在等体积的情况下,其浓度也就越大。标准维生素C溶液中维生素C含量是一定的,我们可以根据向标准维生素C溶液中滴加碘水的量,进而估算出橙汁、果味饮料中维生素C的含量。根据淀粉遇碘水变蓝,进而确定碘水是否与维生素C完全反应(当滴加碘水至刚刚变蓝,说明维生素C与碘水刚好完全 反应)。当然做此实验必须控制以下量:一是每次所用饮料颜色必须相同;二是量取的几种被测试物质的体积必须相同;三是滴加的碘水每滴体积大小必须相同,否则会影响实验结果。但所用反应容器的大小不会影响实验结果。
反应)。当然做此实验必须控制以下量:一是每次所用饮料颜色必须相同;二是量取的几种被测试物质的体积必须相同;三是滴加的碘水每滴体积大小必须相同,否则会影响实验结果。但所用反应容器的大小不会影响实验结果。

 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案一些食物的近似pH如下:
| 食物 | 葡萄汁 | 苹果汁 | 牛奶 | 鸡蛋清 |
| pH | 3.5~4.5 | 2.9~3.3 | 6.3~6.6 | 7.6~8.0 |
下列说法中不正确的是
A.鸡蛋清和牛奶显碱性 B.苹果汁和葡萄汁显酸性
C.苹果汁比葡萄汁的酸性强 D.胃酸过多的人应少饮苹果汁和葡萄汁
 氧化硫气体是造成酸雨的主要气体,其水溶液叫亚硫酸(H2SO3 )。硫化氢(H2S)是一种具有臭鸡蛋气味的剧毒气体,其水溶液叫氢硫酸。已知相同的条件下,氢硫酸的酸性弱于亚硫酸。室温下向饱和的亚硫酸溶液中通入过量的硫化氢气体,反应的化学方程式为:2H2S + H2SO3 === 3S↓ + 3H2O。则下图中溶液的pH随通入硫化氢的体积的变化曲线示意图正确的是 ( )
氧化硫气体是造成酸雨的主要气体,其水溶液叫亚硫酸(H2SO3 )。硫化氢(H2S)是一种具有臭鸡蛋气味的剧毒气体,其水溶液叫氢硫酸。已知相同的条件下,氢硫酸的酸性弱于亚硫酸。室温下向饱和的亚硫酸溶液中通入过量的硫化氢气体,反应的化学方程式为:2H2S + H2SO3 === 3S↓ + 3H2O。则下图中溶液的pH随通入硫化氢的体积的变化曲线示意图正确的是 ( )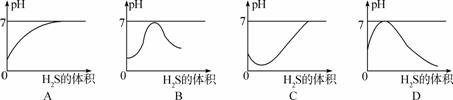
 右图是某补钙剂“高钙片”说明书的一部分。
右图是某补钙剂“高钙片”说明书的一部分。
 ”、“
”、“  ”、“
”、“  ” 分别表示4中不同种类的原子或原子团。该反应属于
” 分别表示4中不同种类的原子或原子团。该反应属于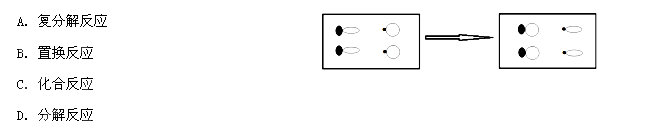
 不稳定: 、
不稳定: 、