题目内容
16.某同学用如图1装置制取氧气,请问答: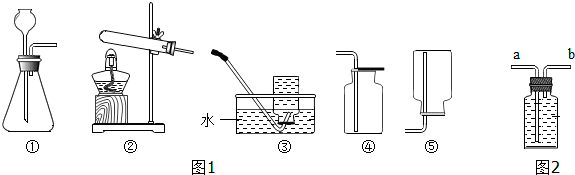
(1)用高锰酸钾制取和收集氧气的装置应选用②③(填序号);写出反应的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;若要制取3.2g氧气,则分解的高锰酸钾的质量至少为31.6g.
(2)实验室为制取较干燥的二氧化碳,用如图2所示装置对制得的气体进行干燥,则该瓶中盛装的是浓硫酸;气体应该从a(填字母序号)端通入.
(3)若用装置③收集的氧气不纯,其原因可能是收集前集气瓶中的水没有装满留有气泡,或没待气泡连续冒出就进行收集等(写一条).
分析 据图即可知道有关仪器的名称,气体的发生装置与反应物的状态和反应的条件有关,气体的收集装置与气体的密度和溶解性有关,根据高锰酸钾受热分解的化学方程式,可得知反应中高锰酸钾与氧气的质量关系,再由生成氧气的质量即可计算所需要高锰酸钾的质量,据此解答.
解答 解:(1)用高锰酸钾制取氧气,是固体加热型反应,应选用的发生装置是②,加热高锰酸钾能生成锰酸钾、二氧化锰和氧气,氧气不易溶于水,收集比较纯净的氧气可以采用排水法进行收集;
设需高锰酸钾的质量为x
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
316 32
x 3.2g
$\frac{316}{x}$=$\frac{32}{3.2g}$ x=31.6g
答:需要高锰酸钾的质量是31.6g
故填:②③,2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;31.6;
(2)浓硫酸有吸水性,洗气应该是长进短出,所以E装置所盛的药品是浓硫酸,气体应由a端通入.
故填:浓硫酸;a;
(3)收集的氧气不纯,其原因可能是:收集前集气瓶中的水没有装满留有气泡,或没待气泡连续冒出就进行收集等.
故填:收集前集气瓶中的水没有装满留有气泡,或没待气泡连续冒出就进行收集等.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
6.如图实验操作错误的是( )
| A. |  加块状固体 | B. |  倾倒液体 | C. |  检查装置气密性 | D. |  加热液体 |
7.化学与人类健康的关系十分密切.下列做法中,不会危害人体健康的是( )
| A. | 用霉变的花生榨取花生油 | |
| B. | 用“干冰”冷藏食品 | |
| C. | 香烟的过滤嘴可滤除CO等有害物质,故吸烟对身体无害 | |
| D. | 青少年正在长身体,应多吃富含蛋白质的肉类,可以不吃蔬菜 |
8.甲、乙两种物质的溶解度曲线如图所示.下列叙述正确的是( )
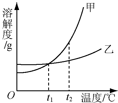

| A. | 依据溶解度曲线可判断,甲的溶解度比乙的大 | |
| B. | 将等质量甲、乙的饱和溶液从t2℃降到t1℃,析出甲的质量小 | |
| C. | 将t2℃时甲的饱和溶液变为不饱和溶液,可采取降温的方法 | |
| D. | 除去甲物质中少量乙物质可采取降温结晶的方法 |
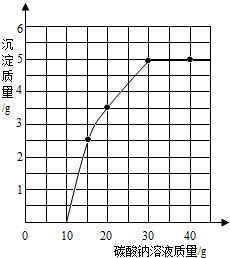 实验室用过量的稀盐酸和大理石制取CO2,取50g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀质量的关系曲线如图所示.
实验室用过量的稀盐酸和大理石制取CO2,取50g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀质量的关系曲线如图所示.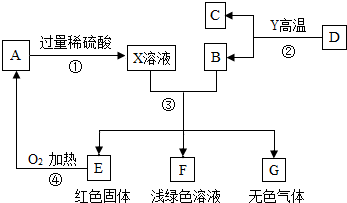 A、B、C、D、E、F、G为初中化学常见的物质,其中B、E、G属于单质,反应②是以赤铁矿为原料炼铁工业中的主要反应,它们之间的相互转化关系如图所示:
A、B、C、D、E、F、G为初中化学常见的物质,其中B、E、G属于单质,反应②是以赤铁矿为原料炼铁工业中的主要反应,它们之间的相互转化关系如图所示: 物质A、B、C是初中化学中常见的物质,A、B、C中都含有一种共同的元素.它们有如图所示的转化关系.回答下列问题:
物质A、B、C是初中化学中常见的物质,A、B、C中都含有一种共同的元素.它们有如图所示的转化关系.回答下列问题: