题目内容
质量相等的锌和铁分别和质量相等、溶质的质量分数也相等的稀盐酸反应,反应情况如图所示.则下列叙述正确的是( )
A.图线a、b表示锌、铁的反应
B.盐酸均反应完,一定有锌剩余
C.盐酸均反应完,一定有铁剩余
D.铁、锌均反应完,盐酸有剩余
【答案】分析:在金属活动性顺序中,越靠前的金属金属活动性越强,和稀酸溶液反应时就越剧烈,则相同质量的金属和同质量、同溶质质量分数的稀酸溶液反应所需的时间也就越少.根据等质量金属完全反应放出氢气质量大小关系:Fe>Zn,若质量相等的锌、铁都完全反应,铁与酸反应放出氢气的量一定大于锌与酸的反应;
解答:解:由图示分析可知两者最终生成的氢气质量相等,所以消耗的酸量一定相等,也就是盐酸一定完全反应,而依据化学方程式的计算可知同质量的铁要比锌生成的氢气要多;
A、因为锌的活动性比铁的活动性强,等质量的金属,锌反应的时间短,因此a代表的是锌,故A正确;
B、由于得到的氢气一样多,说明稀盐酸全部参与反应,而这两种金属都有剩余或铁有剩余,故B错误;
C、由于得到的氢气一样多,说明稀盐酸全部参与反应,而这两种金属都有剩余或铁有剩余,故C正确;
D、由上可知因生成的气体一样多,所以稀盐酸全部参与反应,而铁一定有剩余,故D错误;
故选AC.
点评:本题主要考查了金属的化学性质及其应用,掌握金属活动性顺序及其应用和酸的化学性质;学会利用化学方程式的计算来解决问题.
解答:解:由图示分析可知两者最终生成的氢气质量相等,所以消耗的酸量一定相等,也就是盐酸一定完全反应,而依据化学方程式的计算可知同质量的铁要比锌生成的氢气要多;
A、因为锌的活动性比铁的活动性强,等质量的金属,锌反应的时间短,因此a代表的是锌,故A正确;
B、由于得到的氢气一样多,说明稀盐酸全部参与反应,而这两种金属都有剩余或铁有剩余,故B错误;
C、由于得到的氢气一样多,说明稀盐酸全部参与反应,而这两种金属都有剩余或铁有剩余,故C正确;
D、由上可知因生成的气体一样多,所以稀盐酸全部参与反应,而铁一定有剩余,故D错误;
故选AC.
点评:本题主要考查了金属的化学性质及其应用,掌握金属活动性顺序及其应用和酸的化学性质;学会利用化学方程式的计算来解决问题.

练习册系列答案
相关题目
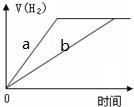 16、质量相等的锌和铁分别和质量相等、溶质的质量分数也相等的稀盐酸反应,反应情况如图所示.则下列叙述错误的是( )
16、质量相等的锌和铁分别和质量相等、溶质的质量分数也相等的稀盐酸反应,反应情况如图所示.则下列叙述错误的是( ) (2013?达州模拟)质量相等的锌和铁分别和质量相等、溶质质量分数也相等的稀盐酸反应,反应情况如右图所示.则下列叙述中正确的是( )
(2013?达州模拟)质量相等的锌和铁分别和质量相等、溶质质量分数也相等的稀盐酸反应,反应情况如右图所示.则下列叙述中正确的是( )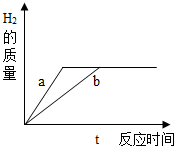
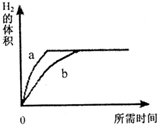 质量相等的锌和铁分别和质量相等、溶质的质量分数也相等的稀盐酸反应,反应情况如图所示.则下列叙述正确的是( )
质量相等的锌和铁分别和质量相等、溶质的质量分数也相等的稀盐酸反应,反应情况如图所示.则下列叙述正确的是( ) (2012?乐山三模)质量相等的锌和铁分别和质量相等、溶质质量分数也相等的稀盐酸反应,反应情况如下图所示.则下列叙述中正确的是( )
(2012?乐山三模)质量相等的锌和铁分别和质量相等、溶质质量分数也相等的稀盐酸反应,反应情况如下图所示.则下列叙述中正确的是( )