题目内容
 如图为哈药集团制药厂生产的“新盖中盖牌”高钙片标签上的部分文字,请仔细阅读后回答下列问题.
如图为哈药集团制药厂生产的“新盖中盖牌”高钙片标签上的部分文字,请仔细阅读后回答下列问题.(1)“新盖中盖牌”高钙片中的“钙”应理解为(填字母)
A.元素 B.原子 C.分子 D.氧化物
(2)人体缺少钙元素会影响健康,因此每日需摄入足够的钙.人体缺钙可能引起的疾病是
(3)碳酸钙CaCO3中Ca、C、O三种元素的质量比为
(4)碳酸钙CaCO3中钙元素的质量分数是多少?(请写出解题过程)
(5)每片钙片中至少含钙元素的质量为多少?(请写出解题过程)
考点:标签上标示的物质成分及其含量,元素的概念,元素质量比的计算,元素的质量分数计算,化合物中某元素的质量计算,人体的元素组成与元素对人体健康的重要作用
专题:标签图示型
分析:(1)食品、药品、营养品、矿泉水等物质中的“钙”等不是以单质、氧化物、分子、原子等形式存在,而是指元素,通常用元素及其所占质量(质量分数)来描述.
(2)根据钙元素对人体健康的作用及元素缺乏症进行解答;
(3)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(4)根据化合物中元素的质量分数计算方法来分析.
(5)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
(2)根据钙元素对人体健康的作用及元素缺乏症进行解答;
(3)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(4)根据化合物中元素的质量分数计算方法来分析.
(5)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答:解:(1))“新盖中盖牌”高钙片中的“钙”不是以单质、氧化物、分子、原子等形式存在,这里所指的“钙”是强调存在的元素,与具体形态无关.故填:A;
(2)人体缺钙可能引起的疾病是佝偻病或骨质疏松等;故填:佝偻病或骨质疏松;
(3)碳酸钙中钙、碳、氧三种元素的质量比为40:12:(16×3)=10:3:16.故填:10:3:16;
(4)碳酸钙中钙元素的质量分数为
×100%=40%;故填:40%;
(5)1片钙片中至少含有1.5g碳酸钙,则1.5g碳酸钙中钙元素的质量为1.5g×40%=0.6g.故填:0.6g.
(2)人体缺钙可能引起的疾病是佝偻病或骨质疏松等;故填:佝偻病或骨质疏松;
(3)碳酸钙中钙、碳、氧三种元素的质量比为40:12:(16×3)=10:3:16.故填:10:3:16;
(4)碳酸钙中钙元素的质量分数为
| 40 |
| 40+12+16×3 |
(5)1片钙片中至少含有1.5g碳酸钙,则1.5g碳酸钙中钙元素的质量为1.5g×40%=0.6g.故填:0.6g.
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
蜡烛(足量)在如下图1密闭的集气瓶内燃烧至熄灭,用仪器测出瓶内氧气含量的变化如图2所示.下列判断正确的是( )
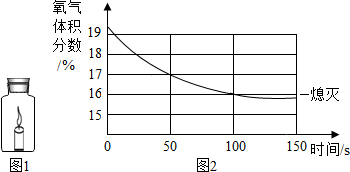

| A、蜡烛燃烧前瓶内只有氧气 |
| B、氧气浓度小于一定值时,蜡烛无法燃烧 |
| C、过程中瓶内物质发生了化合反应 |
| D、蜡烛熄灭后瓶内只剩二氧化碳气体 |
 利用如图探究氧气在空气中的体积含量,下列说法错误的是( )
利用如图探究氧气在空气中的体积含量,下列说法错误的是( )| A、待火焰熄灭,集气瓶冷却至室温后,才能打开止水夹 | ||
B、由实验现象推断氧气在空气中的体积分数大约为
| ||
| C、该实验可说明N2难溶于水 | ||
| D、燃烧匙中的红磷可以换成木炭 |
下列实验内容中,正确的是( )
| A、使用酒精灯火焰的外焰部分给试管内液体加热,并且试管口不能对着人 | ||
| B、把块状固体投入直立的试管中 | ||
| C、用量筒量取液体时,应使视线与量筒内液体的凹液面的最低处保持水平 | ||
D、给试管里的液体加热时,试管里的液体不应超过试管容积的
|
下列实验操作正确的是( )
A、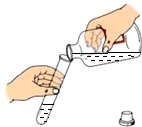 倾倒液体 倾倒液体 |
B、 读取体积 |
C、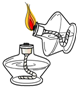 点燃酒精灯 |
D、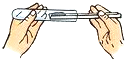 装入固体粉末 |
新发布的《环境空气质量标准》中增加而立PM2.5检测指标,PM2.5是指大气中直径小于或等于2.5微米的颗粒物,对人体健康影响更大,主要来源之一是化石燃料的燃烧,下列措施能减少PM2.5污染的是( )
| A、鼓励开私家车出行 |
| B、鼓励使用太阳能热水器 |
| C、鼓励用煤火力发电 |
| D、鼓励用液化石油气作燃料 |
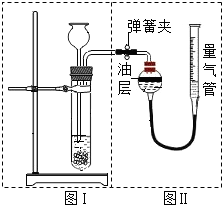 小明设计了如图所示的实验装置来证明氧化铜也能加快过氧化氢溶液的分解,并与相同条件下MnO2的催化效果做比较,实验时间均以生成30mL气体为准(即比较反应的快慢程度).用图示装置测量产生气体的体积,其它可能影响实验因素均已忽略,相关数据如下:
小明设计了如图所示的实验装置来证明氧化铜也能加快过氧化氢溶液的分解,并与相同条件下MnO2的催化效果做比较,实验时间均以生成30mL气体为准(即比较反应的快慢程度).用图示装置测量产生气体的体积,其它可能影响实验因素均已忽略,相关数据如下: