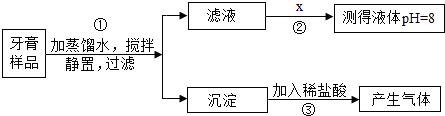
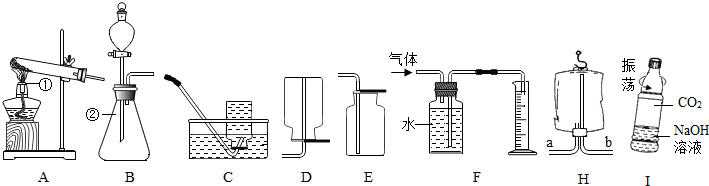
题目内容
13.海盐文化全国知名,某兴趣小组同学去盐场参观,带回了部分粗盐样品,并对其进行了如下探究(如图1所示):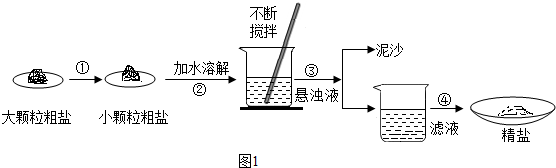
(1)操作①中必须用到的一种仪器是A(填序号).
A.研钵 B.量筒 C.烧杯 D.试管
(2)操作③的名称是过滤,该操作中玻璃棒的作用为引流.
(3)操作④中采用蒸发结晶方法得到精盐(填“蒸发结晶”或“降温结晶”).
(4)查阅资料得知:粗盐中除含少量泥沙等不溶性杂质外,还含有少量的可溶性杂质(假定可溶性杂质只有MgCl2一种),为了得到较纯净的氯化钠,小组同学将所得的“精盐”又作了如图2所示处理:

①白色沉淀的化学式为Mg(OH)2;②在得到的滤液中加入足量的稀盐酸的目的是除去反应剩余的氢氧化钠.
③若实验过程中不考虑损耗,最终到的NaCl固体的质量将大于(填“大于”、“小于”或“等于”)原精盐中NaCl的质量.
分析 (1)根据研钵可以将大块的变成小颗粒的进行分析;
(2)根据过滤可以将不溶物和可溶物分离,以及玻璃棒在过滤过程中的作用进行分析;
(3)根据氯化钠溶解度受温度影响变化不大进行分析;
(4)①根据氢氧化钠和氯化镁会生成氢氧化镁沉淀进行分析;
②根据除去氯化镁加入的氢氧化钠是过量的,对于氯化钠也是杂质进行分析;
③根据氢氧化钠和氯化镁会生成氯化钠,盐酸和氢氧化钠也会生成氯化钠进行分析.
解答 解:(1)研钵可以将大块的变成小颗粒的,所以操作①中必须用到的一种仪器是研钵,故选:A;
(2)过滤可以将不溶物和可溶物分离,所以操作③的名称是过滤,该操作中玻璃棒的作用为引流;
(3)氯化钠溶解度受温度影响变化不大,所以操作④中采用蒸发结晶方法得到精盐;
(4)①氢氧化钠和氯化镁会生成氢氧化镁沉淀,所以白色沉淀的化学式为Mg(OH)2;
②除去氯化镁加入的氢氧化钠是过量的,对于氯化钠也是杂质,所以在得到的滤液中加入足量的稀盐酸的目的是:除去反应剩余的氢氧化钠;
③氢氧化钠和氯化镁会生成氯化钠,盐酸和氢氧化钠也会生成氯化钠,所以实验过程中不考虑损耗,最终到的NaCl固体的质量将大于原精盐中NaCl的质量.
故答案为:(1)A;
(2)过滤,引流;
(3)蒸发结晶;
(4)①Mg(OH)2;
②除去反应剩余的氢氧化钠;
③大于.
点评 本题主要考查了粗盐提纯的相关知识,难度不大,需要在平时多加记忆.

练习册系列答案
相关题目
1.不锈钢是在铁中加入铬镍,改变内部结构,从而起到防锈作用.
小明为了探究铬(Cr)、镁、铜的活动性强弱关系,进行如下探究活动:
【提出假设】对三种金属的活动性顺序提出三种可能的假设:
a.Mg>Cr>Cu b.Mg>Cu>Cr c.Cr>Mg>Cu
【设计实验】同温下,取大小相同的打磨过的金属薄片,分别投入到等体积等浓度的足量稀盐酸中,观察现象,记录如表:
【得出结论】原假设中正确的是b(填假设中a、b或c).
【实验讨论】
(1)铬与盐酸反应的化学方程式是Cr+2HCl═CrCl2+H2↑(Cr在生成物中显+2价),该反应的基本反应类型置换反应
(2)小明还想用硫酸铜溶液代替上述实验中的盐酸,在两试管中分别与镁片、铬片混合得出三种金属的活动性关系.小花认为不可行,理由是无法判断铬和镁的活动性顺序.
【拓展迁移】若只有一支盛有少量稀盐酸的试管,只需合理安排金属片的插入顺序(能与盐酸反应的要一次将盐酸消耗完),也能证明铬、镁、铜这三种金属的活动性顺序,则三金属片的插入顺序为Cu、Cr、Mg.
小明为了探究铬(Cr)、镁、铜的活动性强弱关系,进行如下探究活动:
【提出假设】对三种金属的活动性顺序提出三种可能的假设:
a.Mg>Cr>Cu b.Mg>Cu>Cr c.Cr>Mg>Cu
【设计实验】同温下,取大小相同的打磨过的金属薄片,分别投入到等体积等浓度的足量稀盐酸中,观察现象,记录如表:
| 金属 | Cr | Mg | Cu |
| 与盐酸反应的现象 | 气泡产生缓慢,金属逐渐溶解 | 气泡产生剧烈,金属迅速溶解 | 无气泡产生,金属无变化 |
【实验讨论】
(1)铬与盐酸反应的化学方程式是Cr+2HCl═CrCl2+H2↑(Cr在生成物中显+2价),该反应的基本反应类型置换反应
(2)小明还想用硫酸铜溶液代替上述实验中的盐酸,在两试管中分别与镁片、铬片混合得出三种金属的活动性关系.小花认为不可行,理由是无法判断铬和镁的活动性顺序.
【拓展迁移】若只有一支盛有少量稀盐酸的试管,只需合理安排金属片的插入顺序(能与盐酸反应的要一次将盐酸消耗完),也能证明铬、镁、铜这三种金属的活动性顺序,则三金属片的插入顺序为Cu、Cr、Mg.
2.下列化学用语书写正确的是( )
| A. | 钙离子的符号$\stackrel{+2}{Ca}$ | B. | 硝酸钾的化学式:KNO3 | ||
| C. | 水的化学式:H2O2 | D. | 氧元素的符号:O2 |
3. 如图是工业上在一定条件下制取乙醇反应的微观示意图(其中“○”代表氢原子,“
如图是工业上在一定条件下制取乙醇反应的微观示意图(其中“○”代表氢原子,“ ”代表碳原子,“
”代表碳原子,“ ”代表氧原子).下列叙述中,不正确的是( )
”代表氧原子).下列叙述中,不正确的是( )
 如图是工业上在一定条件下制取乙醇反应的微观示意图(其中“○”代表氢原子,“
如图是工业上在一定条件下制取乙醇反应的微观示意图(其中“○”代表氢原子,“ ”代表碳原子,“
”代表碳原子,“ ”代表氧原子).下列叙述中,不正确的是( )
”代表氧原子).下列叙述中,不正确的是( )| A. | 反应物A的化学符号为2CH2 | |
| B. | 反应前后三种物质的分子个数比为1:1:1 | |
| C. | 乙醇中碳、氢、氧三种元素的质量比为12:3:8 | |
| D. | 1个乙醇分子由1个氧原子、2个碳原子、6个氢原子构成 |