题目内容
7.在AgNO3和Zn(NO3)2的混合溶液中,加入一定量的铁粉充分反应后,过滤、洗涤,将滤渣放入盐酸中有气泡产生,则滤渣成分的组成是( )| A. | Fe、Ag | B. | Fe、Zn | C. | Zn、Ag | D. | Zn、Ag、Fe |
分析 在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,据此进行分析解答.
解答 解:根据在金属活动性顺序中,锌>铁>氢>银,在AgNO3和Zn(NO3)2的混合溶液中,加入一定量的铁粉,故铁粉不能与Zn(NO3)2溶液反应,能与硝酸银反应生成银和硝酸亚铁溶液;充分反应后,过滤、洗涤,将滤渣放入盐酸中有气泡产生,银不与稀盐酸反应,说明滤渣中含有能与稀盐酸反应的金属,该金属应为铁,说明铁是过量的,则滤渣成分的组成是Fe、Ag.
故选:A.
点评 本题难度不是很大,熟练掌握金属的化学性质、综合考虑各种出现的情况是正确解答此类题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.下列变化过程中,一定发生了化学变化的是( )
| A. | 用金刚石切割玻璃 | B. | 食物腐烂 | ||
| C. | 用活性炭净水器净水 | D. | 用汽油清洗油污 |
15.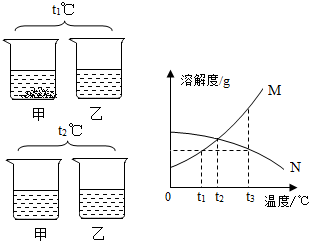 甲、乙两种物质的溶解度曲线如图.t1℃时,在两烧杯中分别加入等质量的两种物质和等质量的蒸馏水,充分溶解后现象如图;继续加热到t2℃时现象如图(不考虑溶剂质量变化).下列说法不正确的是( )
甲、乙两种物质的溶解度曲线如图.t1℃时,在两烧杯中分别加入等质量的两种物质和等质量的蒸馏水,充分溶解后现象如图;继续加热到t2℃时现象如图(不考虑溶剂质量变化).下列说法不正确的是( )
 甲、乙两种物质的溶解度曲线如图.t1℃时,在两烧杯中分别加入等质量的两种物质和等质量的蒸馏水,充分溶解后现象如图;继续加热到t2℃时现象如图(不考虑溶剂质量变化).下列说法不正确的是( )
甲、乙两种物质的溶解度曲线如图.t1℃时,在两烧杯中分别加入等质量的两种物质和等质量的蒸馏水,充分溶解后现象如图;继续加热到t2℃时现象如图(不考虑溶剂质量变化).下列说法不正确的是( )| A. | t1℃时甲一定是饱和溶液 | |
| B. | t2℃时甲、乙两溶液的溶质质量分数相等 | |
| C. | t2℃时甲、乙两溶液一定均为不饱和溶液 | |
| D. | 图中M表示甲的溶解度曲线 |
16.下列实验设计能达到实验目的是( )
| 选项 | 实验目的 | 实验设计 |
| A | 除去粗盐中难溶性杂质 | 将粗盐研碎、溶解、蒸发 |
| B | 除去二氧化碳中少量的水蒸气和氯化氢气体 | 先通过氢氧化钠溶液,再通过浓硫酸 |
| C | 除去硫酸钠溶液中的少量的硫酸 | 向溶液中加入适量的氢氧化钡溶液,过滤 |
| D | 鉴别氯化钠和硝酸铵 | 分别取少量样品,加熟石灰研磨,闻气味 |
| A. | A | B. | B | C. | C | D. | D |