题目内容
9.化学反应往往伴随着一些现象发生,但CO2与NaOH溶液的反应没有明显的现象.为了通过一些现象说明CO2与NaOH发生了反应,某班同学分两组作了如下探究实验:
(1)CO2与NaOH发生了反应的化学方程式为CO2+2NaOH═Na2CO3+H2O
(2)第一组同学把一支收集有CO2的试管倒立在装有饱和NaOH溶液的烧杯中(如图1所示),看到试管内液面上升.这种现象是因为试管内外产生C
A.温度差 B.重力差 C.压强差 D.浮力差
(3)第二组同学从中得到启发,也设计了如上(图A、B、C)实验装置进行探究:
A现象为塑料瓶瘪掉,B现象为熟鸡蛋被吸入瓶中,C现象为气球膨胀变大.
(4)同学们经过分析讨论,认为第一组的实验中产生液面上升现象的原因可能有两种.
一种是因为CO2与溶液中的NaOH反应,消耗了CO2,你认为另一种原因是二氧化碳被水吸收了,为了进一步证实CO2与NaOH溶液已经发生了反应,他们设计了如下方案:取上述实验后的溶液,滴加稀盐酸,现象为有气泡产生 可以证实CO2与NaOH溶液已经发生反应.
分析 验证二氧化碳确实与氢氧化钠发生了反应,只需证明有碳酸钠产生即可.要证明有碳酸钠只需滴加盐酸,若有气泡产生说明二氧化碳确实与氢氧化钠发生了反应,生成了碳酸钠.
解答 解:(1)CO2能与NaOH发生反应生成碳酸钠和水,方程式为CO2+2NaOH═Na2CO3+H2O.
(2)氢氧化钠吸收了二氧化碳气体,使试管内的压强小于大气压强,所以大气压压着液体进入试管.
(3)在A中氢氧化钠吸收了二氧化碳,使塑料瓶内的压强变小,所以塑料瓶变瘪了.在B中氢氧化钠吸收了二氧化碳,使集气瓶内的压强变小,所小鸡蛋被吸进集气瓶.在C中氢氧化钠吸收了二氧化碳后,使烧瓶内的压强减小,所以烧瓶内的气球膨胀.
(4)二氧化碳不但能跟氢氧化钠反应,而且也能溶于水.二氧化碳与氢氧化钠反应生成了碳酸钠,所以可用盐酸来检验是否有碳酸钠.
故答案为:(1)CO2+2NaOH═Na2CO3+H2O;(2)C;(3)塑料瓶瘪掉;熟鸡蛋被吸入瓶中;气球膨胀变大;(4)二氧化碳被水吸收了;稀盐酸;有气泡产生.
点评 二氧化碳与氢氧化钠发生的反应不属于初中任何一种基本反应类型,这是学生经常容易犯错误的地方.

练习册系列答案
相关题目
19.下列物质中,能与稀盐酸反应,但是没有气体放出,也没有沉淀生成的是( )
| A. | Na2CO3 | B. | AgNO3 | C. | Zn | D. | NaOH |
20.我国最近已研究出新型水处理剂C1O2的新制法,其反应的微观过程如图所示.下列说法正确的是( )


| A. | 乙、丙、丁都是混合物 | |
| B. | 该反应属于置换反应 | |
| C. | 该反应符合质量守恒定律 | |
| D. | 该反应的化学方程式为2Cl+2NaClO2=2ClO2+2NaCl |
17.下列过程中主要涉及物理变化的是( )
| A. | 浓硫酸使白纸变黑 | B. | 用浓硫酸来干燥潮湿的氧气 | ||
| C. | 生石灰遇水变成熟石灰 | D. | 盐酸使紫色石蕊溶液变红色 |
14.一次用餐中,小丽同学对“固体酒精”产生好奇,于是她决定买回一袋,对其进行研究.
【收集资料】通过阅读标签及查阅资料,她获得如下信息:
(1)该固体酒精中含有酒精、氢氧化钠等物质.
(2)酒精的化学式为C2H5OH
【提出问题】
(1)酒精的化学式与NaOH相比,都有“OH”,那么酒精的水溶液是不是显碱性?
请同学们帮小丽同学从下面试剂中选择合适试剂进行鉴别AD(填序号)
A.硫酸铜 B.氯化钠 C.硝酸钾 D.酚酞
(2)固体酒精中的氢氧化钠是否变质及变质的程度如何?
【猜想】
猜想一:没有变质,只含有氢氧化钠
猜想二:全部变质,只含有碳酸钠
猜想三:部分变质,含有氢氧化钠和碳酸钠
请写出氢氧化钠在空气中变质的化学方程式CO2+2NaOH=Na2CO3+H2O.
【实验探究】取了少量固体酒精溶于足量水,充分溶解并过滤,取少量上述滤液于试管中,滴入几滴无色酚酞溶液,液体呈红色,甲同学认为固体中含有氢氧化钠,乙同学认为甲同学的结论不正确,其理由是碳酸钠也是呈碱性,能使酚酞变红色.
于是小丽同学和同学们经过讨论并请教老师后,进行了实验探究.请帮她完成下面实验报告(写出详细步骤)
【拓展应用】除去部分变质的氢氧化钠溶液中的杂质,方法是Ca(OH)2+Na2CO3=CaCO3↓+2NaOH或Ba(OH)2+Na2CO3=BaCO3↓+2NaOH(用化学方程式表示).
【收集资料】通过阅读标签及查阅资料,她获得如下信息:
(1)该固体酒精中含有酒精、氢氧化钠等物质.
(2)酒精的化学式为C2H5OH
【提出问题】
(1)酒精的化学式与NaOH相比,都有“OH”,那么酒精的水溶液是不是显碱性?
请同学们帮小丽同学从下面试剂中选择合适试剂进行鉴别AD(填序号)
A.硫酸铜 B.氯化钠 C.硝酸钾 D.酚酞
(2)固体酒精中的氢氧化钠是否变质及变质的程度如何?
【猜想】
猜想一:没有变质,只含有氢氧化钠
猜想二:全部变质,只含有碳酸钠
猜想三:部分变质,含有氢氧化钠和碳酸钠
请写出氢氧化钠在空气中变质的化学方程式CO2+2NaOH=Na2CO3+H2O.
【实验探究】取了少量固体酒精溶于足量水,充分溶解并过滤,取少量上述滤液于试管中,滴入几滴无色酚酞溶液,液体呈红色,甲同学认为固体中含有氢氧化钠,乙同学认为甲同学的结论不正确,其理由是碳酸钠也是呈碱性,能使酚酞变红色.
于是小丽同学和同学们经过讨论并请教老师后,进行了实验探究.请帮她完成下面实验报告(写出详细步骤)
| 实验操作 | 实验现象 | 实验结论 |
| 用试管取少量滤液加入过量的稀盐酸,充分反应 (只能写足量或过量) | 有气泡产生 | 猜想一不成立 |
| 再取少量滤液于试管加入过量的氯化钙溶液,充分反应后,再加入几滴酚酞溶液 | 有白色沉淀产生,溶液变红色(或不变红色) | 则猜想三(或二)成立 |
18.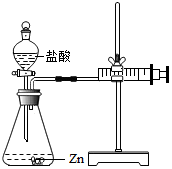 化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.
化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.
【提出问题】金属与盐酸反应剧烈程度受哪些因素的影响?
【作出猜想】
a、可能与金属本身的性质有关
b、可能与盐酸的浓度有关
【设计探究】实验所用金属均已用砂纸打磨.
实验(1)为探究猜想a,小组同学分别在两支试管中放入相同质量的锌片和铁片,然后分别加入相同尝试和质量的稀盐酸,观察到放锌片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡,发生反应的化学方程式有Fe+2HCl=FeCl2+H2↑、Zn+2HCl=ZnCl2+H2↑.
从实验现象可判断:金属活动性Zn>Fe(填“<”“=”“>”).
得出结论:金属与盐酸发生反应的剧烈程度与金属本身性质有关,金属的活动性与反应的剧烈程度的关系是金属与盐酸反应的剧烈程度与金属本身性质有关(金属活动性越强,反应越剧烈).
实验(2)为探究猜想b,小组同学设计如图的装置进行实验,其中注射器的作用是通过注射器往右移动的体积判断生成氢气的体积.所用药品,实验数据如下表:
得出结论:金属与盐酸发生反应的剧烈程度与盐酸的浓度有关,其关系是其他条件相同时,盐酸浓度越大,反应越剧烈.
【反思评价】根据表一中实验Ⅱ数据分析,请描述锌与盐酸发生反应快慢的变化情况并解释原因由慢到快然后逐渐减慢;锌与稀盐酸反应放热,随着反应的进行,温度升高,所以速度越来越快,一段时间后,盐酸被消耗,盐酸浓度变小,反应速率减慢.
通过以上探究,你认为金属与盐酸反应的剧烈程度可能还受哪些因素的影响固体的表面积(写一条即可).
【拓展延伸】很多金属不仅能与酸反应,也能与盐酸溶液反应,现将a g铁钉投入到CuSO4溶液中,反应一段时间后,将固体取出洗净、烘干,称重为b g,则生成铜的质量为8(b-a)g.
 化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.
化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.【提出问题】金属与盐酸反应剧烈程度受哪些因素的影响?
【作出猜想】
a、可能与金属本身的性质有关
b、可能与盐酸的浓度有关
【设计探究】实验所用金属均已用砂纸打磨.
实验(1)为探究猜想a,小组同学分别在两支试管中放入相同质量的锌片和铁片,然后分别加入相同尝试和质量的稀盐酸,观察到放锌片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡,发生反应的化学方程式有Fe+2HCl=FeCl2+H2↑、Zn+2HCl=ZnCl2+H2↑.
从实验现象可判断:金属活动性Zn>Fe(填“<”“=”“>”).
得出结论:金属与盐酸发生反应的剧烈程度与金属本身性质有关,金属的活动性与反应的剧烈程度的关系是金属与盐酸反应的剧烈程度与金属本身性质有关(金属活动性越强,反应越剧烈).
实验(2)为探究猜想b,小组同学设计如图的装置进行实验,其中注射器的作用是通过注射器往右移动的体积判断生成氢气的体积.所用药品,实验数据如下表:
实验编号 | 选用金属(均取2g) | 盐酸质量分数(均取50mL) | 每分钟产生氢气的体积/mL | |||||
| 1分钟 | 1-2分钟 | 2-3分钟 | 3-4分钟 | 4-5分钟 | 前5分钟共收集气体 | |||
| Ⅰ | 锌片 | 15% | 2.9 | 16.9 | 11.0 | 9.2 | 7.6 | 48.5 |
| Ⅱ | 锌片 | 5% | 1.6 | 8.4 | 5.9 | 4.8 | 3.7 | 24.4 |
【反思评价】根据表一中实验Ⅱ数据分析,请描述锌与盐酸发生反应快慢的变化情况并解释原因由慢到快然后逐渐减慢;锌与稀盐酸反应放热,随着反应的进行,温度升高,所以速度越来越快,一段时间后,盐酸被消耗,盐酸浓度变小,反应速率减慢.
通过以上探究,你认为金属与盐酸反应的剧烈程度可能还受哪些因素的影响固体的表面积(写一条即可).
【拓展延伸】很多金属不仅能与酸反应,也能与盐酸溶液反应,现将a g铁钉投入到CuSO4溶液中,反应一段时间后,将固体取出洗净、烘干,称重为b g,则生成铜的质量为8(b-a)g.
 化学概念间有包含、并列、交叉等不同关系.下列选项符合如图所示关系的是( )
化学概念间有包含、并列、交叉等不同关系.下列选项符合如图所示关系的是( )