题目内容
8.有一包白色固体,可能由BaCl2、CuSO4、KNO3、Na2O中的一种或几种物质组成.更具下图所示的变化和实验现象进行推断.
试判断固体中一定含有CuSO4、Na2O;一定不含BaCl2;可能含有KNO3.
写出①、②发生反应的化学方程式.①Na2O+H2O=2NaOH、CuSO4+2NaOH=Cu(OH)2↓+Na2SO4 .
②Na2SO4+Ba(NO3)2=BaSO4↓+2NaNO3.
分析 依据初中化学范围中蓝色沉淀一般是氢氧化铜,而滴加硝酸酸化的硝酸钡后能够生成白色沉淀可知该沉淀是硫酸钡,滴加硝酸酸化硝酸银没有沉淀生成可知该溶液中没有氯离子分析解答即可;
解答 解:初中范围内蓝色沉淀一般是氢氧化铜,固体加水后能够生成蓝色沉淀氢氧化铜,可知原固体中含有硫酸铜,同时也含有氧化钠与水反应生成的氢氧化钠,该过程中没有白色沉淀生成,则说明没有氯化钡(硫酸铜和氯化钡能够生成白色的硫酸钡沉淀);过滤后滴加硝酸银和稀硝酸出现白色沉淀,则进一步证明溶液中含有硫酸根离子,无色溶液滴加硝酸银和稀硝酸没有沉淀生成,则说明溶液中没有氯离子,故原固体中没有氯化钡,依据以上的分析可知对硝酸钾的有误无法判断;
则:固体中一定含有硫酸铜、氧化钠,一定不含氯化钡,可能含有硝酸钾;
①、②发生反应的化学方程式为:①Na2O+H2O=2NaOH、CuSO4+2NaOH=Cu(OH)2↓+Na2SO4,②Na2SO4+Ba(NO3)2=BaSO4↓+2NaNO3;
故答案为:CuSO4、Na2O; BaCl2;KNO3;Na2O+H2O=2NaOH、CuSO4+2NaOH=Cu(OH)2↓+Na2SO4 ;Na2SO4+Ba(NO3)2=BaSO4↓+2NaNO3;
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后结合题中的现象分析各种物质的存在性,最后确定混合物的成分.

练习册系列答案
相关题目
1.下列物质间的转化,只有通过加入盐溶液才能一步实现的是( )
| A. | Fe→FeCl2 | B. | CuO→CuCl2 | C. | CaCO3→CaCl2 | D. | K2SO4→KCl |
5.下列除杂(括号内为杂质)方法错误的是( )
| A. | CO(CO2):将气体通过澄清石灰水,然后干燥 | |
| B. | CO2(CO):将气体点燃 | |
| C. | 食盐(泥沙):溶解、过滤 | |
| D. | Cu(Fe):用磁铁吸引 |
20.正确的操作是实验成功的关键之一,以下操作正确的是( )
| A. | 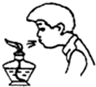 熄灭酒精灯 | B. |  闻气味 | ||
| C. | 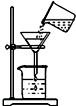 过滤 | D. | 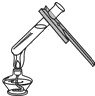 给试管里的液体加热 |
18.下列各项中:①原子的数目,②分子数目,③元素的种类,④原子的种类,⑤物质的种类,在化学变化中,肯定没有变化的是( )
| A. | ①④⑤ | B. | ①②④ | C. | ①③④ | D. | ①③④⑤ |
 氢氧化铜是一种常用的杀菌剂,常见的剂型有77%氢氧化铜可湿性粉剂、37.5%氢氧化铜悬浮剂、25%氢氧化铜悬浮剂.为了回收氢氧化铜,现向含CuCl2和HCl的100g混合溶液中,逐滴加溶质质量分数为10%的NaOH溶液,发生反应:CuCl2+2NaOH═2NaCl+Cu(OH)2↓.参加反应的NaOH溶液质量与生成沉淀质量关系如图.据图回答:
氢氧化铜是一种常用的杀菌剂,常见的剂型有77%氢氧化铜可湿性粉剂、37.5%氢氧化铜悬浮剂、25%氢氧化铜悬浮剂.为了回收氢氧化铜,现向含CuCl2和HCl的100g混合溶液中,逐滴加溶质质量分数为10%的NaOH溶液,发生反应:CuCl2+2NaOH═2NaCl+Cu(OH)2↓.参加反应的NaOH溶液质量与生成沉淀质量关系如图.据图回答: 如图中A烧杯盛有浓氨水,B烧杯内是滴加了几滴酚酞溶液的蒸馏水.过一会儿,观察到的现象是酚酞溶液变红,本实验能说明分子不断运动(答出一条即可).
如图中A烧杯盛有浓氨水,B烧杯内是滴加了几滴酚酞溶液的蒸馏水.过一会儿,观察到的现象是酚酞溶液变红,本实验能说明分子不断运动(答出一条即可).