题目内容
1.世界是物质的,物质都是由化学元素组成的.到目前为止,已经发现自然界中存在的和实验室合成的物质超过三千万种,并且化学家还在以每年近百万种的速度继续发现更多的新物质.请你运用所学的知识在下表空白处填上适当的内容:| 物质名称 | 物质组成 (用化学式表示) | 构成物质的微粒 (用符号表示) | 物质中各元素的质量比 |
| 氧气 | O2 | ||
| 过氧化氢 | mH:mO=1:l6 | ||
| 熟石灰 | Ca(OH)2 |
分析 应利用分子、原子、离子、元素与物质之间的关系及元素质量比的有关知识进行计算.
解答 解:氧气、过氧化氢都是由分子构成的,熟石灰是由离子构成的.
构成氧气的微粒是氧分子,其符号为:O2;
过氧化氢是由显+1价的氢元素和显-1价的氧元素组成,其化学式为:H2O2;构成过氧化氢的微粒是过氧化氢分子,其符号为:H2O2;
其中氢元素和氧元素的质量比为:(1×2):(16×2)=1:16;
熟石灰是氢氧化钙的俗称,氢氧化钙是由显+2价的钙元素和显-1价的氢氧根组成,其化学式为:Ca(OH)2;它是由钙离子和氢氧根离子构成的,其符号分别为:Ca2+、OH-;氢氧化钙中含有三种元素,其质量比为Ca:O:H=40:(16×2):(1×2)=20:16:1;
故答案为:
| 物质名称 | 物质组成 (用化学式表示) | 构成物质的微粒 (用符号表示) | 物质中各元素的质量比 |
| 氧气 | O2 | ||
| 过氧化氢 | H2O2 | H2O2 | mH:mO=1:l6 |
| 熟石灰 | Ca2+、OH-; | mCa:mO:mH=20:16:1 |
点评 熟练掌握化学式的书写和物质的构成和元素质量比的计算方法是解决此题的关键.

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
16.某同学发现化肥袋上有一标签,如图1所示:
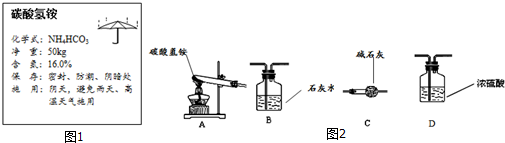
根据图示回答下列问题:
(1)碳酸氢铵是由4 种元素组成的,各元素的质量比N:H:C:O为14:5:12:48.
(2)写出碳酸氢铵的一点化学性质受热易分解.
【提出问题】
A.为什么要避免高温天气使用?
B.这种化肥含氮量是否达到16%,化肥中碳酸氢铵的含量是多少?
带着这些问题,她取了一些化肥样品,进入实验室.
【查找资料】
A.碱石灰能够吸收水和二氧化碳,但是不吸收氨气. B.浓硫酸能吸收氨气.
【性质实验探究】
她设计了如图2的实验装置:
(3)用A装置给碳酸氢铵加热,装药品前,她必须进行的一步操作是检查装置的气密性.
(4)取少量碳酸氢铵加入试管,加热,闻到刺激性气味,此气体化学式为NH3.
(5)连接A、B装置,继续加热,试管口出现小水珠,同时观察到B中的现象是变浑浊.
(6)碳酸氢铵在受热时发生反应的文字或符号表达式是NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+CO2↑+H2O.
【含量分析】
将装置A、C、D依次连接,加入10g化肥样品,加热至A中固体质量不再改变.
她称量装置D的质量如表:
(7)由此分析得知:反应中产生氨气的质量为1.7g,其中氮元素的质量为1.4g.
(8)通过反应的表达式可以知道:氨气中氮元素全部来自于碳酸氢铵(假设杂质中不含氮元素),请计算此化肥含氮量为14%.(用百分数表示)
(9)请计算此化肥中碳酸氢铵的质量分数(表示写出计算过程).

根据图示回答下列问题:
(1)碳酸氢铵是由4 种元素组成的,各元素的质量比N:H:C:O为14:5:12:48.
(2)写出碳酸氢铵的一点化学性质受热易分解.
【提出问题】
A.为什么要避免高温天气使用?
B.这种化肥含氮量是否达到16%,化肥中碳酸氢铵的含量是多少?
带着这些问题,她取了一些化肥样品,进入实验室.
【查找资料】
A.碱石灰能够吸收水和二氧化碳,但是不吸收氨气. B.浓硫酸能吸收氨气.
【性质实验探究】
她设计了如图2的实验装置:
(3)用A装置给碳酸氢铵加热,装药品前,她必须进行的一步操作是检查装置的气密性.
(4)取少量碳酸氢铵加入试管,加热,闻到刺激性气味,此气体化学式为NH3.
(5)连接A、B装置,继续加热,试管口出现小水珠,同时观察到B中的现象是变浑浊.
(6)碳酸氢铵在受热时发生反应的文字或符号表达式是NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+CO2↑+H2O.
【含量分析】
将装置A、C、D依次连接,加入10g化肥样品,加热至A中固体质量不再改变.
她称量装置D的质量如表:
| 实验前D装置的质量 | 150g |
| 实验后D装置的质量 | 151.7g |
(8)通过反应的表达式可以知道:氨气中氮元素全部来自于碳酸氢铵(假设杂质中不含氮元素),请计算此化肥含氮量为14%.(用百分数表示)
(9)请计算此化肥中碳酸氢铵的质量分数(表示写出计算过程).
6.下列实验方案中,设计合理的是( )
| A. | 鉴别黄铜(铜锌合金)和黄金:用硫酸锌溶液来鉴别 | |
| B. | 除去铜粉中的木炭粉:将混合物在空气中充分灼烧 | |
| C. | 制取少量硫酸亚铁溶液:将过量的铁粉与稀硫酸混合充分反应后,过滤 | |
| D. | 分离铜和银的固体混合物:加入适量硝酸银溶液,过滤,洗涤,烘干 |
13.食物较长时间露置在空气中就会变质,这主要是由于空气中含有( )
| A. | 氧气 | B. | 氮气 | C. | 二氧化碳 | D. | 水蒸气 |
10.上海世博会于10月31日闭幕,在闭幕式上的精彩表演中,发生化学变化的是( )
| A. | 焰火表演 | B. | 霓虹灯表演 | C. | 音乐喷泉 | D. | 气球升空 |
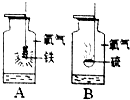 如图是有关氧气化学性质的两个实验,根据题意,回答下列问题:
如图是有关氧气化学性质的两个实验,根据题意,回答下列问题: