题目内容
1.甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示.下列叙述正确的是( )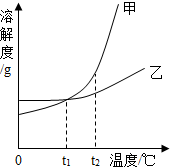
| A. | t1℃时,甲和乙溶液中溶质的质量分数一定相等 | |
| B. | t2℃时,分别用等质量的甲和乙固体,完全溶解配制成饱和溶液,得到乙溶液的质量大于甲 | |
| C. | 将甲、乙的饱和溶液从t1℃升温至t2℃,甲溶液中溶质的质量分数比乙大 | |
| D. | 使甲的不饱和溶液变成饱和溶液只能用降温的方法 |
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
A、不知溶液中溶质、溶剂的质量多少,无法判断溶质的质量分数是否相等;
B、据该温度下甲乙的溶解度大小及溶解度概念分析解答;
C、据饱和时质量分数的计算式$\frac{溶解度}{100g+溶解度}$×100%解答;
D、根据不饱和溶液转化为饱和溶液的方法解答.
解答 解:A、不知溶液中溶质、溶剂的质量多少,无法判断溶质的质量分数是否相等;据饱和时质量分数的计算式$\frac{溶解度}{100g+溶解度}$×100%可知:若两溶液是饱和溶液,该温度下二者的溶解度相等,则溶质的质量分数相等;故错误;
B、t2℃时甲的溶解度大于乙,即等质量的水中溶解的甲大于乙,所以用等质量的甲和乙固体配制饱和溶液,需要水的质量甲小于乙,得到乙溶液的质量大于甲;故正确;
C、t1℃时的甲、乙的溶解度相等,溶质的质量分数相等,分别将t1℃时的甲、乙的饱和溶液升温至t2℃,甲和乙的溶解度均增大,但是溶液组成不变,故溶质的质量分数均不变,故错误;
D、甲的不饱和溶液变成饱和溶液可以加溶质、蒸发溶剂,还可以用降温的方法,故错误.
答案:B、
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
11.2015年10月中国药学家屠呦呦发现抗疟疾青蒿素而获得诺贝尔生活学或医学家,下列有关青蒿素(C15H22O5)的说法不正确的是( )
| A. | 青蒿素由碳、氢、氧三种元素组成 | |
| B. | 青蒿素是由15个碳原子、22个氢原子和5个氧原子构成 | |
| C. | 青蒿素中碳、氢、氧三种元素的质量比为15:22:5 | |
| D. | 青蒿素是一种有机化合物 |
12.下列物质的俗名与化学式不一致的是( )
| A. | NaCl:食盐 | B. | CaO:生石灰 | C. | CuSO4:胆矾 | D. | Ca(OH)2:消石灰 |
9.下列过程属于化学变化的是( )
| A. | 蔗糖溶于水形成溶液 | B. | 木炭燃烧 | ||
| C. | 分离液态空气制取氧气 | D. | 海水晒盐 |
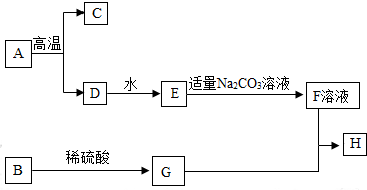
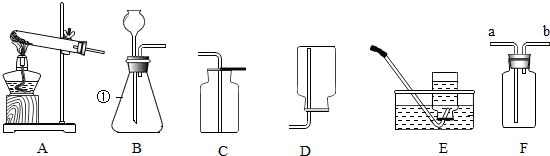
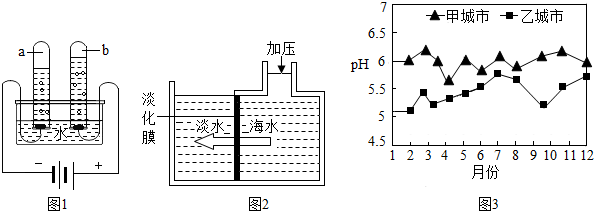
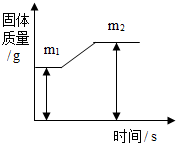 质量守恒定律是一条重要规律,请利用该规律的相关知识回答下列问题.
质量守恒定律是一条重要规律,请利用该规律的相关知识回答下列问题.