题目内容
6.一包白色粉末,可能由硫酸铜、碳酸钙、氯化钡、硫酸钠和氢氧化钠中的两种或两种以上的物质混合而成.为探究其组成,某同学进行如下实验:(1)取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液.则原白色粉末中一定不含有CuSO4.(填化学式,下同)
(2)取实验(1)滤出的白色沉淀,向其中加入足量的稀盐酸,沉淀全部溶解,并产生无色气体.则原白色粉末中一定含有CaCO3.
(3)取实验(2)反应后得到的残液,向其中加入硝酸银溶液和足量的稀硝酸,有白色沉淀产生.则由此不能(填“能”或“不能”)判断原白色粉末中一定含有氯化钡,理由是氯化钙能和硝酸银反应生成不溶于稀硝酸的白色沉淀氯化银.
根据上述(1)~(3)实验可推断:原白色粉末的组成有5(填数字)种可能.
分析 根据硫酸铜在溶液中显蓝色,碳酸钙不溶于水,溶于酸,硫酸钠和氯化钡会生成不溶于酸的硫酸钡沉淀,根据这些知识进行分析.
解答 解:硫酸铜在溶液中显蓝色,碳酸钙不溶于水,溶于酸,硫酸钠和氯化钡会生成不溶于酸的硫酸钡沉淀.
(1)取一定量的白色粉末加入足量的水并充分搅拌,过滤,得到白色沉淀I和无色滤液I,所以混合物中一定不含硫酸铜;
(2)在白色沉淀I中加入足量稀盐酸,白色沉淀全部溶解,得到无色气体,所以产生的沉淀一定是碳酸钙;
(3)取实验(2)反应后得到的残液,向其中加入硝酸银溶液和足量的稀硝酸,有白色沉淀产生,不能确定一定含有氯化钡,因为(2)中加入盐酸,产生的氯化钙能与硝酸银反应产生氯化银沉淀;
由此推断:白色粉末成分的可能组合为:碳酸钙、氢氧化钠或碳酸钙、氯化钡或碳酸钙、硫酸钠或碳酸钙、氢氧化钠、硫酸钠.
故答案为:(1)CuSO4;
(2)CaCO3;
(3)不能;氯化钙能和硝酸银反应生成不溶于稀硝酸的白色沉淀氯化银;5.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
16.下列性质是溶液的基本特征的是( )
| A. | 无色 | B. | 透明 | C. | 纯净 | D. | 均一、稳定 |
14.下列说法正确的是( )
| A. | 可以食用甲醛溶液浸泡的海产品 | |
| B. | 吃水果和蔬菜可以补充维生素 | |
| C. | 生活污水不是化工废水,可向江河湖泊里任意排放 | |
| D. | 用活性炭可以降低水的硬度 |
1.为了响应武汉市政府“2016年拥抱蓝天行动方案”,下列做法不合理的是( )
| A. | 取缔中心城区露天烧烤 | |
| B. | 城市新建项目可以配套建设自备燃煤电站 | |
| C. | 严禁农作物秸秆和垃圾露天焚烧 | |
| D. | 夜间渣土运输车必须经过无尘处理 |
11.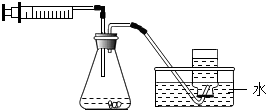 在实验室里,利用下列物质和装置制取气体的方法正确的是( )
在实验室里,利用下列物质和装置制取气体的方法正确的是( )
 在实验室里,利用下列物质和装置制取气体的方法正确的是( )
在实验室里,利用下列物质和装置制取气体的方法正确的是( )| A. | 二氧化锰和氯酸钾制取氧气 | B. | 大理石和稀盐酸制取二氧化碳 | ||
| C. | 大理石与稀硫酸制取二氧化碳 | D. | 锌和稀硫酸制取氢气 |
16.除去下列各物质中的少量杂质,所选用的试剂、方法均正确的是( )
| 编号 | 物质 | 杂质(少量) | 试剂 | 除杂操作方法 |
| A | Fe | Cu | 足量稀盐酸 | 过滤、烘干 |
| B | NaOH | Na2CO3 | 适量的稀盐酸 | 蒸发 |
| C | CO2 | CO | -- | 点燃 |
| D | NaCl | NaOH | 足量稀盐酸 | 蒸发 |
| A. | A | B. | B | C. | C | D. | D |
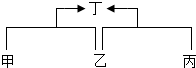 已知甲、乙、丙、丁是初中化学中的四种常见物质,丁是甲与乙、乙与丙反应的生成物之一(反应条件均已略去),转化关系如图:
已知甲、乙、丙、丁是初中化学中的四种常见物质,丁是甲与乙、乙与丙反应的生成物之一(反应条件均已略去),转化关系如图: