题目内容
9.按要求写出下列文字表达式(1)产生有刺激性气味的化合反应硫+氧气$\stackrel{点燃}{→}$二氧化硫.
(2)剧烈燃烧、火星四射的化合反应铁+氧气$\stackrel{点燃}{→}$四氧化三铁.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据文字表达式的书写方法、步骤(将反应物和生成物的名称分别写在式子的左、右两边,并在式子的左、右两边之间标出一个指向生成物的箭头;当反应物或生成物有多种时,中间用“+”连接起来)进行书写即可.
解答 解:(1)硫在空气中燃烧生成二氧化硫,是产生有刺激性气味的化合反应,反应的文字表达式为:硫+氧气$\stackrel{点燃}{→}$二氧化硫.
(2)铁丝在氧气中燃烧生成四氧化三铁,是剧烈燃烧、火星四射的化合反应,反应的文字表达式为:铁+氧气$\stackrel{点燃}{→}$四氧化三铁.
故答案为:(1)硫+氧气$\stackrel{点燃}{→}$二氧化硫;(2)铁+氧气$\stackrel{点燃}{→}$四氧化三铁.
点评 本题难度不大,考查学生根据反应原理书写文字表达式的能力,掌握文字表达式的书写方法即可正确解答本题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.某校化学兴趣小组就空气中氧气的含量进行实验探究:
【集体讨论】:
(1)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其它成分反应,而且生成物为固体.他们应该选择(填编号)B.
A.蜡烛 B.红磷 C.硫粉

为了充分消耗容器中的氧气,药品的用量应保证足量.水B水A
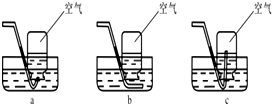
(2)小组同学共同设计了如下图的两套装置,你认为合理的是(填编号)A.为了确保实验的成功,在装药品之前应该检查装置气密性.
【分组实验】在讨论的基础上,他们分组进行了实验.
[数据分析]实验结束后,整理数据如下:(注:集气瓶容积为100mL)
(3)根据燃烧红磷测定空气中氧气含量的实验原理是红磷燃烧消耗氧气,生成固体,使容器内体积减小、压强减小.
【分组讨论】
(4)第三组同学进入集气瓶中水的体积明显比其他组同学少,原因是(答一条)红磷的量太少、装置漏气
第五组同学进入集气瓶中水的体积明显比其他组同学多,原因是(答一条)弹簧夹没有夹紧或点燃红磷伸入瓶中没有立即塞紧瓶塞
(5)通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的$\frac{1}{5}$.
【实验总结】
(6)小组的同学反思上述实验的探究过程后认为:用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的要求上应考虑的是药品要能在空气中燃烧时只消耗氧气;生成物是固体.
【集体讨论】:
(1)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其它成分反应,而且生成物为固体.他们应该选择(填编号)B.
A.蜡烛 B.红磷 C.硫粉

为了充分消耗容器中的氧气,药品的用量应保证足量.水B水A
(2)小组同学共同设计了如下图的两套装置,你认为合理的是(填编号)A.为了确保实验的成功,在装药品之前应该检查装置气密性.
【分组实验】在讨论的基础上,他们分组进行了实验.
[数据分析]实验结束后,整理数据如下:(注:集气瓶容积为100mL)
| 组 别 | 1 | 2 | 3 | 4 | 5 | 6 |
| 进入集气瓶中水的体积(mL) | 20 | 21 | 14 | 20 | 28 | 19 |
【分组讨论】
(4)第三组同学进入集气瓶中水的体积明显比其他组同学少,原因是(答一条)红磷的量太少、装置漏气
第五组同学进入集气瓶中水的体积明显比其他组同学多,原因是(答一条)弹簧夹没有夹紧或点燃红磷伸入瓶中没有立即塞紧瓶塞
(5)通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的$\frac{1}{5}$.
【实验总结】
(6)小组的同学反思上述实验的探究过程后认为:用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的要求上应考虑的是药品要能在空气中燃烧时只消耗氧气;生成物是固体.
1. 通过初中化学的学习,我们知道通过多种途径可制取氧气.
通过初中化学的学习,我们知道通过多种途径可制取氧气.
A.加热氧化汞 B.分离空气 C.电解水D.加热分解KMnO4E.分解H2O2F.加热分解KClO3;
(1)请你在F处再写出一种制取氧气的方法.
(2)请写出一个实验室制取氧气的文字表达式:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.
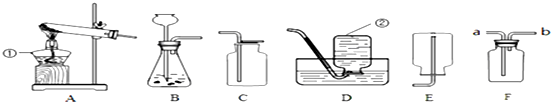
(3)若用如图装置加热高锰酸钾制取氧气,指出装置中的三处明显的错误:导气管插入试管太长、试管口向上倾斜、试管口没有棉花.
(4)实验完毕,停止加热前应该先将导气管移出水面,再移走酒精灯(合理表述均可).
(5)实验室还能用向上排空气方法收集氧气,理由是氧气的密度比空气的大.
(6)以下是某研究小组探究影响化学反应快慢的一些因素的相关数据(常温通常指20℃;“浓度”指溶质的质量分数)
①过实验①和②对比可知,化学反应快慢与过氧化氢的浓度有关;
②通过对比实验③和④可知,化学反应快慢与温度的关系是温度越高反应速度越快,温度越低反应速度越慢.
③由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是20℃时5%过氧化氢溶液中加入少量二氧化锰.
 通过初中化学的学习,我们知道通过多种途径可制取氧气.
通过初中化学的学习,我们知道通过多种途径可制取氧气.A.加热氧化汞 B.分离空气 C.电解水D.加热分解KMnO4E.分解H2O2F.加热分解KClO3;
(1)请你在F处再写出一种制取氧气的方法.
(2)请写出一个实验室制取氧气的文字表达式:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.
(3)若用如图装置加热高锰酸钾制取氧气,指出装置中的三处明显的错误:导气管插入试管太长、试管口向上倾斜、试管口没有棉花.
(4)实验完毕,停止加热前应该先将导气管移出水面,再移走酒精灯(合理表述均可).
(5)实验室还能用向上排空气方法收集氧气,理由是氧气的密度比空气的大.
(6)以下是某研究小组探究影响化学反应快慢的一些因素的相关数据(常温通常指20℃;“浓度”指溶质的质量分数)
| 实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液质量/g | 温度/℃ | 二氧化锰用量/g | 氧气体积/ml | 反应所需时间/s |
| ① | 5 | 12 | 20 | 0.2 | 125 | 11 |
| ② | 30 | 12 | 20 | 0.2 | 125 | 2 |
| ③ | 30 | 12 | 40 | / | 125 | 148 |
| ④ | 30 | 12 | 90 | / | 125 | 82 |
②通过对比实验③和④可知,化学反应快慢与温度的关系是温度越高反应速度越快,温度越低反应速度越慢.
③由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是20℃时5%过氧化氢溶液中加入少量二氧化锰.
18.如图是稀HCl和NaOH溶液反应的pH变化曲线图,据图分析能得出的结论正确的是( ) 

| A. | 该反应是NaOH溶液中滴入稀盐酸 | |
| B. | a克是指加入NaOH溶液的质量 | |
| C. | A点时,溶液中的溶质只有NaCl | |
| D. | B点表示稀盐酸和加入的NaOH溶液质量相等时 |