题目内容
14.如图是某化学兴趣小组的同学对氢氧化钠部分性质的探究过程: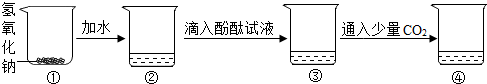
(1)用手触摸②的烧杯外壁,感觉发烫,这是由于氢氧化钠固体溶于水时会放热(填“吸热”或“放热”),该溶液呈无色;③中的溶液显红色.
(2)从③到④溶液的颜色变化不明显,说明④中的溶液呈碱性(填“酸”或“碱”),④中发生反应的化学方程式为CO2+2NaOH═Na2CO3+H2O.
分析 (1)根据氢氧化钠溶解于水放热、溶液无色、氢氧化钠的碱性分析;
(2)根据指示剂的变色反应分析;二氧化碳与氢氧化钠反应是碳酸钠和水.
解答 解:(1)氢氧化钠固体溶解于水放热、溶液呈无色、氢氧化钠的溶液呈碱性,能使酚酞溶液变红;
(2)溶液颜色仍显红色,说明二氧化碳和氢氧化钠反应后的溶液仍然显碱性;二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,反应的化学方程式为:CO2+2NaOH═Na2CO3+H2O.
故答案为:(1)放热;无;红;
(2)碱;CO2+2NaOH═Na2CO3+H2O.
点评 本题主要考查常见的碱,了解常见碱的种类及性质,是解决问题的前提.

练习册系列答案
相关题目
9.下列物质能用于鉴别氢氧化钠溶液和稀盐酸的是( )
| A. | 氯化钠溶液 | B. | CO2 | C. | 澄清石灰水 | D. | 铁粉 |
6.“美丽厦门,共同缔造”.下列回收物品中属于有机合成材料的是( )
| A. | 废金属 | B. | 旧报纸 | C. | 塑料瓶 | D. | 玻璃瓶 |
4.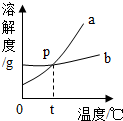 运用氯化钠和硝酸钾的溶解度表和溶解度曲线回答下列问题.
运用氯化钠和硝酸钾的溶解度表和溶解度曲线回答下列问题.
(1)a表示硝酸钾(或KNO3) 的溶解度曲线.
(2)曲线上p点表示的意义是t℃时,a、b两物质的溶解度相等.
(3)60℃时,50g水中加入60g硝酸钾固体,所得溶液的质量为105g.
 运用氯化钠和硝酸钾的溶解度表和溶解度曲线回答下列问题.
运用氯化钠和硝酸钾的溶解度表和溶解度曲线回答下列问题.| 温度/℃ | 30 | 40 | 50 | 60 | |
| 溶解度/g | 氯化钠 | 36.3 | 36.6 | 37.0 | 37.3 |
| 硝酸钾 | 45.8 | 63.9 | 85.5 | 110 | |
(2)曲线上p点表示的意义是t℃时,a、b两物质的溶解度相等.
(3)60℃时,50g水中加入60g硝酸钾固体,所得溶液的质量为105g.