题目内容
现有下列物质:
a、铁粉b、锌粉c、铜粉d、盐酸e、硝酸f、硫酸g、氢氧化钡 h、石灰水 i、氢氧化铁 j、碳酸钙k、氯酸钾l、高锰酸钾
从上述物质中选取适当的物质,按下表要求填空.
a、铁粉b、锌粉c、铜粉d、盐酸e、硝酸f、硫酸g、氢氧化钡 h、石灰水 i、氢氧化铁 j、碳酸钙k、氯酸钾l、高锰酸钾
从上述物质中选取适当的物质,按下表要求填空.
| 实验要求 | 选取物质(填编号) | 化学方程式 |
| 除去氯化锌溶液里混有的少量氯化铜杂质 | ||
| 一定条件下分解一种物质,使生成物既有碱性氧化物,又有酸性氧化物 | ||
| 选用一种试剂可以区分碳酸钠、硝酸钡、硝酸钠三种无色溶液 |
考点:化学实验方案设计与评价,盐的化学性质,酸、碱、盐的鉴别,书写化学方程式、文字表达式、电离方程式
专题:简单实验方案的设计与评价
分析:用化学方法除杂质的原理是添加合适的试剂,让杂质与所加试剂反应,将杂质除去,加入的试剂只与杂质反应,不与原物反应,反应后不能引入新的杂质.区分不同的物质时,选择适当的试剂进行试验,要求能出现不同的现象.书写化学方程式时要注意化学式的写法,配平和条件等.
解答:解:氯化铜会与锌发生置换反应生成氯化锌和铜,通过过滤可以将铜出去,而剩下氯化锌,能除去杂质且没有引入新的杂质.分析所给的物质,能一定条件下分解,生成物既有碱性氧化物,又有酸性氧化物的是碳酸钙,它分解能生成氧化钙和二氧化碳,氧化钙是碱性氧化物,二氧化碳的酸性氧化物;用一种试剂可以区分碳酸钠、硝酸钡、硝酸钠三种无色溶液,可选用硫酸,硫酸和碳酸钠反应生成气体,和硝酸钡反应生成沉淀,和硝酸钠不反应,没有现象,故可以区分.
故答案为:
故答案为:
| 选取物质(填编号) | 化学方程式 | |||||
| b | Zn+CuCl2═ZnCl2+Cu | |||||
| j | CaCO3
| |||||
| f | Na2CO3+H2SO4=Na2SO4+H2O+CO2↑; H2SO4+Ba(NO3)2═BaSO4↓+2HNO3 |
点评:此题主要考查物质间的相互反应的现象以及方程式的书写,进而归纳反应的特点和规律,属于基础知识,难度中等.

练习册系列答案
相关题目
下列物质的化学式书写正确的是( )
| A、硫酸铁:FeSO4 |
| B、氧化铝:Al2O3 |
| C、氯化钙:CaCl |
| D、氢氧化钙:CaOH |
如图所示是两种气体发生反应的微观示意图,其中相同颜色的球代表同种原子.下列说法正确的是( )


| A、原子在化学反应中可分 |
| B、化学反应前后原子的种类不变 |
| C、分子在化学变化中不可分 |
| D、反应后生成了两种新的物质 |
 为了研究质量守恒定律,设计了如图“红磷燃烧前后质量测定”的实验,请分析有关问题:
为了研究质量守恒定律,设计了如图“红磷燃烧前后质量测定”的实验,请分析有关问题: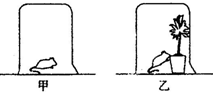 英国科学家普利斯特里曾做过一个实验.如图,在密闭玻璃容器甲内放一只小白鼠,在另一密闭玻璃容器乙内放一盆绿色植物和一只小白鼠,分别给予足够的光照,发现小白鼠在乙容器中比在甲容器中存活的时间长得多.此实验说明,植物在进行光合作用时会释放出
英国科学家普利斯特里曾做过一个实验.如图,在密闭玻璃容器甲内放一只小白鼠,在另一密闭玻璃容器乙内放一盆绿色植物和一只小白鼠,分别给予足够的光照,发现小白鼠在乙容器中比在甲容器中存活的时间长得多.此实验说明,植物在进行光合作用时会释放出