题目内容
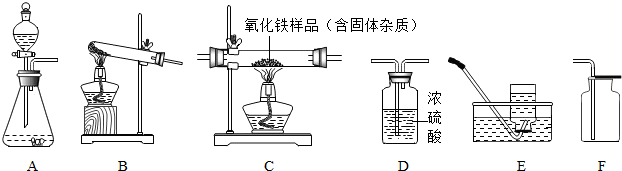
11.某兴趣小组同学对实验室制取氧气的条件进行如下探究实验.(1)为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比试验:
Ⅰ.将3.0g KClO3与1.0gMnO2均匀混合加热
Ⅱ.将xg KClO3与1.0gCuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.
Ⅰ中反应的化学方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;Ⅱ中χ的值为3.0.
(2)乙探究了影响双氧水分解速度的某种因素,实验数据记录如表:
| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2的体积 | |
| Ⅰ | 50.0g | 1% | 0.1g | 9mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16mL |
| Ⅲ | 50.0g | 4% | 0.1g | 31mL |
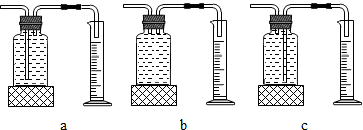
实验结论:在相同条件下,双氧水浓度越大,双氧水分解越快.
分析 根据已有的知识进行分析,(1)氯酸钾在二氧化锰的催化作用下加热能快速的产生氧气,进行实验探究时要注意控制变量,
(2)测量氧气的体积可以使用排水法,将排出的水的用量筒收集起来,排出的水的体积就是氧气的体积;根据表格数据即可得出影响反应速率的因素.
解答 解:(1)氯酸钾在二氧化锰的催化作用下加热能快速的产生氧气,进行实验探究时要注意控制变量,氯酸钾的质量需要相同,故X为3.0,故填:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,3.0;
(2)要将瓶内的水排出来,与量筒相连的导管应该伸到瓶底,a和b都不可以,c可以,故填:c;
根据表格提供的数据可以看出,双氧水的浓度越大,相同的时间产生氧气的体积越大,故填:双氧水浓度越大.
点评 本题考查了影响化学反应速率的因素,完成此题,可以依据题干提供的信息结合已有的知识进行.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
1.下列实验操作错误的是( )
| A. |  氧气验满 | B. |  收集二氧化碳气体 | ||
| C. |  倾倒液体 | D. |  检查装置气密性 |
16.为实现下列实验目的,所选的试剂或方法正确的是( )
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 区分真金和假金(铜锌合金) | 用硫酸铝溶液鉴别 |
| B | 除去硫酸亚铁溶液中含有的硫酸铜 | 加足量的铁粉,过滤 |
| C | 除去CO2中的CO气体 | 在氧气中点燃 |
| D | 除去氯化钠溶液中的碳酸钠溶液 | 加入足量稀盐酸,过滤 |
| A. | A | B. | B | C. | C | D. | D |
20.为除去物质中的杂质(括号内为杂质),所选试剂(过量)及操作方法均正确的是( )
| 物质 | 选用试剂 | 操作方法 | |
| A | Cu(CuO) | 氧气 | 通入氧气并加热 |
| B | KCl(KClO3) | 二氧化锰 | 加入MnO2后加热,使之充分反应 |
| C | FeCl2溶液(CuCl2) | 铁 | 加入铁充分反应后过滤 |
| D | KCl溶液(K2CO3) | 氯化钙溶液 | 加入氯化钙溶液充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |