题目内容
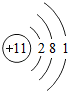
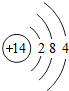
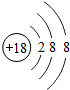
如图给出了部分元素的原子结构示意图:| 纵列 横行 | 1 | 8 | ||||||
| 一 | 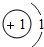 | 2 | 3 | 4 | 5 | 6 | 7 | 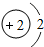 |
| 二 | 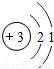 | 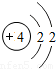 | 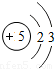 | 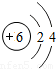 | 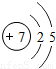 | 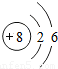 | 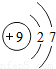 | 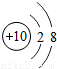 |
| 三 | 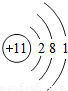 | 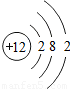 | 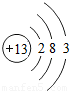 | 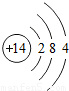 | 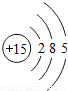 | 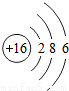 | x | 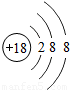 |
①同一横行(称为周期)的元素,其原子具有相同的 ,不同的 ;
②同一纵列(称为族)的元素,其原子具有相同的 ,不同的 ;
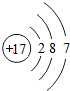
(2)根据图中电子排布的规律,画出元素“X”的原子结构示意图为 ;
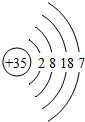
(3)溴(Br)元素的原子结构示意图为
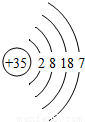 ,它与图中第 列元素的化学性质最相似.溴与金属元素化合时的化合价为 ;溴化钠的化学式为 .
,它与图中第 列元素的化学性质最相似.溴与金属元素化合时的化合价为 ;溴化钠的化学式为 .
【答案】分析:(1)根据同一横行和同一纵行中原子结构示意图分析相同点和不同点
(2)根据元素周期表排列依据及原子结构示意图各部分含义分析
(3)最外层电子数决定元素的化学性质.
解答:解:(1)①由每一横行的元素的原子结构示意图可以看出,每一横行中原子具有相同的 电子层数最外层电子数不同;
②同一纵列的元素,原子具有相同的 最外层电子数,不同的 电子层数;
(2)元素周期表是按照原子序数递增顺序排列的,因此X的质子数17,原子结构示意图为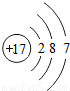 ;
;
(3)溴(Br)元素的原子结构示意图可知最外层电子数为7,图中第 7列元素的最外层电子数也为7,它们的化学性质最相似.最外层为7个电子,在形成化合物时易得到一个电子显价,溴化钠中钠元素为+1价,溴元素为-1价,化学式为 NaBr.
故答案为:(1)①电子层数,最外层电子数;②最外层电子数,电子层数;
(2)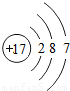 ;(3)7-1价; NaBr.
;(3)7-1价; NaBr.
点评:本题考查元素周期表的特点及原子结构示意图中各部分含义,属于基础知识考查.
(2)根据元素周期表排列依据及原子结构示意图各部分含义分析
(3)最外层电子数决定元素的化学性质.
解答:解:(1)①由每一横行的元素的原子结构示意图可以看出,每一横行中原子具有相同的 电子层数最外层电子数不同;
②同一纵列的元素,原子具有相同的 最外层电子数,不同的 电子层数;
(2)元素周期表是按照原子序数递增顺序排列的,因此X的质子数17,原子结构示意图为
 ;
;(3)溴(Br)元素的原子结构示意图可知最外层电子数为7,图中第 7列元素的最外层电子数也为7,它们的化学性质最相似.最外层为7个电子,在形成化合物时易得到一个电子显价,溴化钠中钠元素为+1价,溴元素为-1价,化学式为 NaBr.
故答案为:(1)①电子层数,最外层电子数;②最外层电子数,电子层数;
(2)
 ;(3)7-1价; NaBr.
;(3)7-1价; NaBr.点评:本题考查元素周期表的特点及原子结构示意图中各部分含义,属于基础知识考查.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
如图给出了部分元素的原子结构示意图:
| 纵列 横行 | 1 | 8 | ||||||
| 一 | 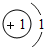 | 2 | 3 | 4 | 5 | 6 | 7 | 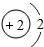 |
| 二 | 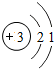 | 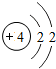 | 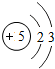 | 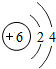 | 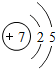 | 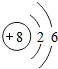 | 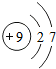 |  |
| 三 | 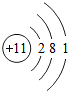 | 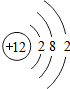 | 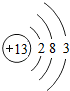 | 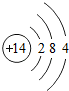 |  | 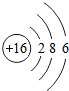 | x | 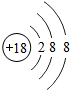 |
①同一横行(称为周期)的元素,其原子具有相同的______,不同的______;
②同一纵列(称为族)的元素,其原子具有相同的______,不同的______;
(2)根据图中电子排布的规律,画出元素“X”的原子结构示意图为______;
(3)溴(Br)元素的原子结构示意图为
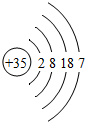 ,它与图中第______列元素的化学性质最相似.溴与金属元素化合时的化合价为______;溴化钠的化学式为______.
,它与图中第______列元素的化学性质最相似.溴与金属元素化合时的化合价为______;溴化钠的化学式为______.
如图给出了部分元素的原子结构示意图:
(1)仔细分析图中电子排布的规律可以发现:
①同一横行(称为周期)的元素,其原子具有相同的 ,不同的 ;
②同一纵列(称为族)的元素,其原子具有相同的 ,不同的 ;
(2)根据图中电子排布的规律,画出元素“X”的原子结构示意图为 ;
(3)溴(Br)元素的原子结构示意图为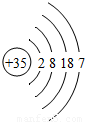 ,它与图中第 列元素的化学性质最相似.溴与金属元素化合时的化合价为 ;溴化钠的化学式为 .
,它与图中第 列元素的化学性质最相似.溴与金属元素化合时的化合价为 ;溴化钠的化学式为 .
| 纵列 横行 | 1 | 8 | ||||||
| 一 | 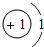 | 2 | 3 | 4 | 5 | 6 | 7 | 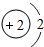 |
| 二 | 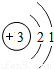 | 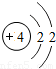 | 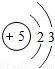 | 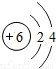 | 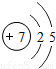 | 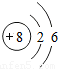 | 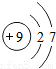 | 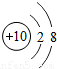 |
| 三 | 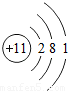 | 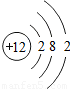 | 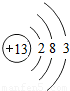 | 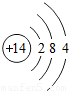 | 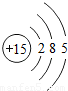 | 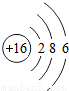 | x | 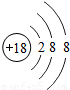 |
①同一横行(称为周期)的元素,其原子具有相同的 ,不同的 ;
②同一纵列(称为族)的元素,其原子具有相同的 ,不同的 ;
(2)根据图中电子排布的规律,画出元素“X”的原子结构示意图为 ;
(3)溴(Br)元素的原子结构示意图为
 ,它与图中第 列元素的化学性质最相似.溴与金属元素化合时的化合价为 ;溴化钠的化学式为 .
,它与图中第 列元素的化学性质最相似.溴与金属元素化合时的化合价为 ;溴化钠的化学式为 .  32、自然环境是由生物圈、岩石圈、大气圈、水圈组成的.
32、自然环境是由生物圈、岩石圈、大气圈、水圈组成的.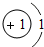
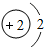
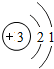
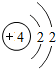
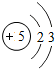
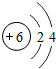
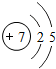
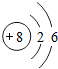
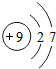
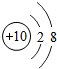

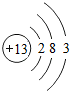
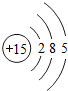
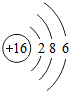
 ,它与图中第
,它与图中第