题目内容
19.为提高实验探究能力,某化学兴趣小组的同学在老师的指导下,对一瓶久置出现变质硬化的氢氧化钙固体进行如下探究活动.【探究活动一】试验硬化的氢氧化钙样品是否完全变质
(1)用化学方程式表示氢氧化钙变质的原因:CO2+Ca(OH)2═CaCO3↓+H2O.
(2)检验氢氧化钙样品是否完全变质,进行如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取氢氧化钙样品少量,研细后加适量蒸馏水 充分混合后静置,取少量上层清液,滴加1~2滴无色酚酞试液(或其他合理答案) | 溶液变成红色(或其他合理答案) | 该样品还含有氢氧化钙 |
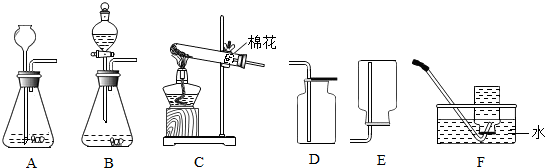
取3克部分变质的氢氧化钙样品与足量的稀盐酸反应,测量生成气体的体积(气体不溶于植物油),从而计算出样品中R的质量,便可求出样品中R的质量分数.实验装置(气密性良好)如图1所示.

(3)将稀盐酸滴入样品中,产生气体的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑,反应一段时间后,当观察到无气泡产生(填实验现象),才停止滴加稀盐酸.
(4)实验中量筒的作用是根据进入量筒内水的体积,测量生成的CO2的体积(或其他合理答案).
(5)实验结束后,量筒内进入水的体积如图2所示,其读数为165mL.已知在该实验条件下,生成气体的密度为2g•L-1,通过计算,样品中R的质量分数为25%.
(6)上述图1所示实验装置和相关试剂,用来实验测定样品中R的质量分数是比较粗略的,请简要说明测定数据存在误差的原因:无法考虑盐酸加入后烧瓶内物质所占体积的变化对测定数据产生的影响(或其他合理答案)(写一个).
分析 (1)根据氢氧化钙和二氧化碳反应产生碳酸钙沉淀和水写出反应的方程式;
(2)根据氢氧化钙溶液显碱性设计实验并描述现象;
(3)根据碳酸钙和盐酸反应产生氯化钙、水和二氧化碳,写出反应的方程式并描述现象;
(4)根据实验目的分析量筒的作用;
(5)根据量筒的读数方法读数并进行化学方程式的计算;
(6)根据实验目的分析可能产生的误差原因.
解答 解:(1)氢氧化钙和二氧化碳反应产生碳酸钙沉淀和水,故反应的方程式为:CO2+Ca(OH)2═CaCO3↓+H2O;
(2)氢氧化钙溶液显碱性,能够使酚酞试液变成红色,因此可以取少量上层清液,滴加1~2滴无色酚酞试液(或其他合理答案);溶液变成红色(或其他合理答案);故答案为:取少量上层清液,滴加1~2滴无色酚酞试液(或其他合理答案);溶液变成红色(或其他合理答案);
(3)滴加稀盐酸和碳酸钙反应产生二氧化碳,至不再产生气泡时说明碳酸钙反应完全,碳酸钙和盐酸反应产生氯化钙、水和二氧化碳;故答案为:CaCO3+2HCl═CaCl2+H2O+CO2↑;无气泡产生;
(4)要测定反应产生二氧化碳的体积,通过气压的增大把水压入量筒,量筒内水的体积就是二氧化碳的体积;故答案为:根据进入量筒内水的体积,测量生成的CO2的体积(或其他合理答案);
(5)读数时视线与凹液面的最低处保持水平,因此读数为165mL,即0.165L,二氧化碳的密度为2g•L-1,因此二氧化碳的质量为0.33g.
设碳酸钙的质量分数为x,则样品中碳酸钙的质量为3xg,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
3xg 3.3g
$\frac{100}{3xg}$=$\frac{44}{3.3g}$ x=25%
故答案为:165;25%;
(6)在实验过程中无法考虑盐酸加入后烧瓶内物质所占体积的变化对测定数据产生的影响,可能会对测定样品中R的质量分数产生一定的影响;
故答案为:无法考虑盐酸加入后烧瓶内物质所占体积的变化对测定数据产生的影响(或其他合理答案).
点评 本题从定性和定量的两个角度探究了氢氧化钙的变质程度及变质程度的计算,难度较大,解题的关键是明确氢氧化钙、碳酸钙等的性质及测定的原理.

 阅读快车系列答案
阅读快车系列答案| 选项 | 事 实 | 解 释 |
| A | 食盐在冷水中溶解得更慢 | 氯化钠分子运动速率随温度降低而减慢 |
| B | 夏天氦气球在阳光下曝晒过久易爆炸 | 氦原子间的间隔随温度的升高而增大 |
| C | 一氧化碳有可燃性而二氧化碳不可燃 | 构成分子的原子的种类不同 |
| D | 氢氧化钾溶液能使紫色石蕊溶液变蓝 | 在水中会解离出钾离子和氢氧根离子 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 乘坐公共交通工具携带酒精 | |
| B. | 炒菜时油锅着火用锅盖盖灭 | |
| C. | 液化气着火,首先迅速关闭液化气罐阀门 | |
| D. | 火场逃生时在有烟雾的地方匍匐前进 |
| A. | 镁粉、氧化铜粉、木炭粉 | B. | NaOH溶液、Ba(OH)2溶液、KOH溶液 | ||
| C. | Na2CO3溶液、NaCl溶液、BaCl2溶液 | D. | 铝片、铁片、银片 |
 黑龙江绿色食品闻名全国,近几年推出的蓝莓系列产品因其天然健康的品质,深受大家的喜爱
黑龙江绿色食品闻名全国,近几年推出的蓝莓系列产品因其天然健康的品质,深受大家的喜爱