题目内容
根据下表信息,完成表中空格:
化学符号 | 2H | ______ | Mg2+ | ________ |
符号的意义 | ___ | 2个氮分子 | ______ | 五氧化二磷中磷元素的化合价为+5价 |
 2个氢原子 2N2 镁离子
【解析】
化学符号
2H
2N2
Mg2+
符号的意义
2个氢原子
2个氮分子
镁离子
五氧化二磷中磷元素的化合价为+5价
点睛∶本题主要考查化学式的意义,特别需要区别化合价和离子的表示不同。
2个氢原子 2N2 镁离子
【解析】
化学符号
2H
2N2
Mg2+
符号的意义
2个氢原子
2个氮分子
镁离子
五氧化二磷中磷元素的化合价为+5价
点睛∶本题主要考查化学式的意义,特别需要区别化合价和离子的表示不同。
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案物质的性质决定用途.下列是物质的一些性质:①密度小,很稳定、②有吸附性、③有导电性、④易升华、⑤能与酸反应.请选择恰当的数字序号填空.
用途 | 石墨作电极芯 | 活性炭用于防毒面具
| 氦气用于探空气球
| 碳酸氢钠用于面点发酵
| 干冰用于人工降雨
|
性质 | (1)石墨___ | (2)活性炭______ | (3)氦气_________ | (4)碳酸氢钠_______ | (5)干冰_______ |
A、B、C、D、E为初中化学常见的五种物质,它们之间有如图所示的转化和反应关系(“→”表示某一种物质经一步反应可转化为另一种物质,“—”表示相连两物质能发生化学反应,部分反应物、生成物及反应条件己略去)。

⑴若A的固体可用于人工降雨,B为植物光合作用的产物之一,E在工业上广泛用于玻璃、造纸、纺织和洗涤剂的生产等。则B为__________;D与E反应的基本类型为___________
⑵若A为人体胃酸的士要成分,D与E经混合研磨可产生刺激性气味的气体,且图中体现了A的四种不同化学性质。则C物质的类别是__________;D与E反应的化学方程式为___________________________。
 氧气或O2复分解反应氧化物NaOH+NH4Cl=NaCl+NH3↑+H2O[或Ca(OH)2+NH4Cl=CaCl2+2NH3↑+2H2O]
【解析】
(1)若A的固体可用于人工降雨,B为植物光合作用的产物之一,E在工业上广泛用于玻璃、造纸、纺织和洗涤剂的生产等,可知A是二氧化碳,B可以为氧气,E为碳酸钠;二氧化碳能够和氢氧化钙反应,氢氧化钙能够和碳酸钠反应,经过验证,推导正确,因此B...
氧气或O2复分解反应氧化物NaOH+NH4Cl=NaCl+NH3↑+H2O[或Ca(OH)2+NH4Cl=CaCl2+2NH3↑+2H2O]
【解析】
(1)若A的固体可用于人工降雨,B为植物光合作用的产物之一,E在工业上广泛用于玻璃、造纸、纺织和洗涤剂的生产等,可知A是二氧化碳,B可以为氧气,E为碳酸钠;二氧化碳能够和氢氧化钙反应,氢氧化钙能够和碳酸钠反应,经过验证,推导正确,因此B... 下列有关水的说法中,不正确的是
A.水是一种常用的溶剂 B.保护水资源是全人类的责任
C.常用肥皂水来鉴别硬水和软水 D.电解水得到的氧气和氢气的体积比为2:1
 D
【解析】A、水是最常见的溶剂,正确;B、水资源是有限的,要爱护水资源,正确;C、鉴别硬水和软水用到的是肥皂水,加肥皂水搅拌,若是软水会产生大量的泡沫,若是硬水则泡沫较少并会产生大量的浮杂,正确;D、电解水实验中与正极产生的是氧气,用带火星的小木条检验,负极产生的是氢气,可用燃烧法检验,正负两极气体的体积比为1:2 ,错误。故选D。
D
【解析】A、水是最常见的溶剂,正确;B、水资源是有限的,要爱护水资源,正确;C、鉴别硬水和软水用到的是肥皂水,加肥皂水搅拌,若是软水会产生大量的泡沫,若是硬水则泡沫较少并会产生大量的浮杂,正确;D、电解水实验中与正极产生的是氧气,用带火星的小木条检验,负极产生的是氢气,可用燃烧法检验,正负两极气体的体积比为1:2 ,错误。故选D。 这幅卡通画形象地展现了钠与氯气反应形成氯化钠的微观过程,在此过程中,钠原子变成了钠离子。

钠原子和氯原子的结构示意图分别为:
(1)钠元素处于周期表中第____________周期。
(2)氯元素是非金属元素,它的原子一般在反应中容易____________电子。
(3)请你比较分析钠原子、钠离子的异同。
相同之处:①______________;②____________。
不同之处:①____________;②_____________。
 三得到核内质子数 ;中子数 。核外电子总数 ;最外层电子数
【解析】
根据周期数等于电子层数,最外层电子数大于4个时在发生化学变化时易得电子及钠原子和钠离子的微粒结构的示意图来解答。
(1)在元素周期表中,周期数等于电子层数,钠原子的核外有三个电子层,所以在第三周期;
(2)氯元素的最外层有7个电子,在化学变化中易得到电子;
(3)比较钠原子和钠离子的微粒结构,可以看...
三得到核内质子数 ;中子数 。核外电子总数 ;最外层电子数
【解析】
根据周期数等于电子层数,最外层电子数大于4个时在发生化学变化时易得电子及钠原子和钠离子的微粒结构的示意图来解答。
(1)在元素周期表中,周期数等于电子层数,钠原子的核外有三个电子层,所以在第三周期;
(2)氯元素的最外层有7个电子,在化学变化中易得到电子;
(3)比较钠原子和钠离子的微粒结构,可以看... 下列涉及学科观点的有关说法正确的是
A. 根据微粒观:水是由氢原子和氧原子构成的
B. 根据转化观:一氧化碳和二氧化碳在一定条件下可相互转化
C. 根据结构观:氩原子和氯离子最外层电子数相同,化学性质相同
D. 根据守恒观:10mL质量分数40%的硫酸,加10mL水后质量分数变为20%
 B
【解析】
水由水分子构成,不是由原子直接构成;氩原子和氯离子的化学性质不同,氯离子可以结合阳离子构成化合物,而氩原子性质稳定;10mL质量分数40%的硫酸质量大于10g,10mL水的质量等于10g,混合后质量分数大于平均值20%,等质量混合时才是20%。
B
【解析】
水由水分子构成,不是由原子直接构成;氩原子和氯离子的化学性质不同,氯离子可以结合阳离子构成化合物,而氩原子性质稳定;10mL质量分数40%的硫酸质量大于10g,10mL水的质量等于10g,混合后质量分数大于平均值20%,等质量混合时才是20%。 作为相对原子质量标准的1个碳原子的质量是1.993×10-26kg,一种氢原子1个原子的质量为 3.348×10-27kg,则该氢原子的相对原子质量为
A.1 B.2 C.3 D.4
 B
【解析】
试题相对原子质量等于原子的实际质量和碳原子质量的十二分之一的比值,因此为
B
【解析】
试题相对原子质量等于原子的实际质量和碳原子质量的十二分之一的比值,因此为 下列图像分别与选项中的操作相对应,其中不合理的是( )
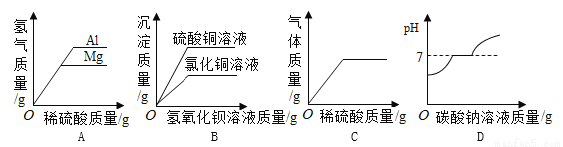
A. 分别向 5 g 镁粉和 5 g 铝粉中滴加足量稀硫酸
B. 分别向相同质量和浓度的氯化铜和硫酸铜溶液中滴加氢氧化钡溶液
C. 向氢氧化钠和碳酸钠的混合溶液中滴加稀硫酸
D. 向氯化钙和盐酸的混合溶液中滴加碳酸钠溶液
 C
【解析】
根据各个反应的进程,结合图像进行分析。
A、根据化学方程式2Al + 3H2SO4 === Al2(SO4)3 + 3H2↑可知每18份质量的铝会生成2份质量的氢气,根据化学方程式Mg + H2SO4 === MgSO4 + H2↑每24份质量的镁会生成2份质量的氢气,所以分别向5 g镁粉和铝粉中滴加足量的稀硫酸,铝生成的氢气多,与图像相符,故A正确;B、硫酸铜和氢...
C
【解析】
根据各个反应的进程,结合图像进行分析。
A、根据化学方程式2Al + 3H2SO4 === Al2(SO4)3 + 3H2↑可知每18份质量的铝会生成2份质量的氢气,根据化学方程式Mg + H2SO4 === MgSO4 + H2↑每24份质量的镁会生成2份质量的氢气,所以分别向5 g镁粉和铝粉中滴加足量的稀硫酸,铝生成的氢气多,与图像相符,故A正确;B、硫酸铜和氢... a、b、c三种物质的溶解度曲线如右图所示,下列说法不正确的是
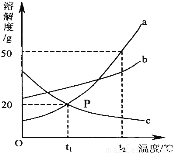
A. t1℃时,等质量的a、c饱和溶液中溶质的质量相等
B. 加水或升温均可使b的饱和溶液变为不饱和溶液
C. 将相同质量的固体a、b溶解配制成t2℃时的饱和溶液,得到的溶液质量为a>b
D. a物质中混有少量c,可采用冷却热饱和溶液的方式提纯a
 C
【解析】
t1℃时,a与c物质的溶解度相同,故相同质量的饱和溶液中溶质的质量相等,A选项正确;加水稀释b溶液,可使其由饱和溶液变为不饱和溶液,升温溶解度增大,可使其由饱和溶液变为不饱和溶液,B选项正确;由于t2℃时a的溶解度>b的溶解度,故将相同质量的固体a、b溶解配制成饱和溶液,得到溶液的质量a<b,C选项错误;a的溶解度随温度的升高而增大,c的溶解度随温度的升高而减小,应该用冷...
C
【解析】
t1℃时,a与c物质的溶解度相同,故相同质量的饱和溶液中溶质的质量相等,A选项正确;加水稀释b溶液,可使其由饱和溶液变为不饱和溶液,升温溶解度增大,可使其由饱和溶液变为不饱和溶液,B选项正确;由于t2℃时a的溶解度>b的溶解度,故将相同质量的固体a、b溶解配制成饱和溶液,得到溶液的质量a<b,C选项错误;a的溶解度随温度的升高而增大,c的溶解度随温度的升高而减小,应该用冷...