题目内容
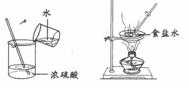
氨气易溶于水,易与浓硫酸反应,不与碱石灰(干燥剂)反应。氨气还具有还原性,在加热的条件下能还原氧化铜:2NH3 + 3CuO N2 + 3Cu + 3H2O ,某化学兴趣小组同学设计下图所示实验来验证氨气的组成(图中夹持、固定装置部分均略去)。已知整套装置气密性良好,且实验中所用试剂均足量,B、D、E中所装药品能完全吸收相关物质。实验前装置 C、D 的质量分别为 mC1、mD1 .
N2 + 3Cu + 3H2O ,某化学兴趣小组同学设计下图所示实验来验证氨气的组成(图中夹持、固定装置部分均略去)。已知整套装置气密性良好,且实验中所用试剂均足量,B、D、E中所装药品能完全吸收相关物质。实验前装置 C、D 的质量分别为 mC1、mD1 .

实验步骤:
I. 连接装置A、B、C、D、E,打开分液漏斗旋塞注入足量浓氨水后关闭旋塞。通人氨气一段时间后,接着连接装置F。
Ⅱ.点燃酒精灯加热,待黑色固体变为红色后,停止加热。
Ⅲ.继续通氨气至玻璃管冷却。
Ⅳ.记录量气管读数为 V mL。
V.称量装置 C、D 的质量分别为 mC2、mD2 .
请回答下列问题:
⑴装置A中NaOH固体所起的作用,是利用了该物质 的性质。
⑵若 mC1 - mC2 = (mD2 - mD1)× ,则可证明氨气的组成中不含氧元素。
⑶步骤 Ⅲ 通入氨气的目的之一是 。
⑷如果略去装置B,导致的后果是 。
①装置C中会发生新的化学反应
②会得出“氨气的组成中含有氧元素”的结论
③使测得的氨气组成中N、H元素质量比偏大
⑸为减小误差,在读取量气管读数前必须进行的操作是 。
⑹步骤Ⅱ中氧化铜是否完全反应,对实验结果 (填“有”、“没有”或“不确定有没有”)影响。
⑴遇水溶解放热
⑵ 8/9(或16/18)
⑶排出装置内生成物,减小误差(或防止浓硫酸倒吸)
⑷ ②
⑸调节水准管,使量气管与水准管液面相平
⑹没有

金属钠在空气中极易被氧化,常温下能与水剧烈反应生成氢氧化钠和氢气.化学兴趣小组同学在老师指导下设计了下图所示装置进行实验探究(支持装置已略去)。已知:该装置气密性良好;煤油不与金属钠反应;煤油密度比水小且不溶于水。
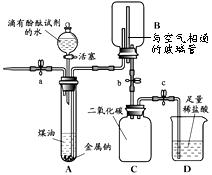
有关实验操作及现象记录如下:
| 步骤 | 操 作 | 现 象 |
| I | 先打开a,再打开分液漏斗活塞。待大试管A中充满液体后,立即关闭a及分液漏斗活塞 | A中液体分层,油层在上。钠熔成银白色小球,在液体的界面处剧烈反应,产生大量气泡;下层溶液呈红色,并逐渐进入B中 |
| II | 打开b,待B中部分溶液进入C中时关闭b,并打开a排气减压 | C中溶液仍呈红色 |
| III | 打开止水夹c | D中溶液进入C中,产生气泡,溶液变为无色 |
下列关于该实验的说法:
①步骤I、II中红色溶液呈碱性,步骤I II中无色溶液呈中性
II中无色溶液呈中性
②步骤III中,C装置内发生的化学反应有1个 或2个
或2个
③本实验证明了二氧化碳能与氢氧化钠起反应
④装置D中若改用氯化钙溶液也能实现实验探究的目的
⑤装置B中与空气相通的玻 璃管的主要作用是维持内外气压平衡,使液体顺利地进出
璃管的主要作用是维持内外气压平衡,使液体顺利地进出
其中错误说法的个数是
A.1 B.2 C.3 D.4
 X
X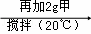 Y
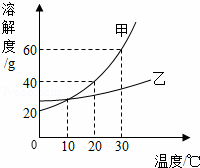
Y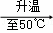 Z为饱和溶液的是 (填“X”或“Y”或“Z”);若三中溶液中溶质的质量分数分别为a、b、c,则它们的大小关系是 (用“<”或“>”或“=”表示出来)
Z为饱和溶液的是 (填“X”或“Y”或“Z”);若三中溶液中溶质的质量分数分别为a、b、c,则它们的大小关系是 (用“<”或“>”或“=”表示出来)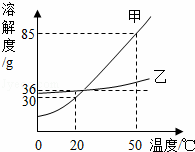
 的海产品对人体无害
的海产品对人体无害 解,小苏打易分解,反应的化学方程式为:2NaHCO3
解,小苏打易分解,反应的化学方程式为:2NaHCO3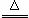 Na2CO3 + CO2↑ + H2O 。碱石灰是CaO与NaOH的固体混合物;已知,该装置气密性良好,A、C、D中所装药品足量且能完全吸收相关物质。探究过程如下:
Na2CO3 + CO2↑ + H2O 。碱石灰是CaO与NaOH的固体混合物;已知,该装置气密性良好,A、C、D中所装药品足量且能完全吸收相关物质。探究过程如下: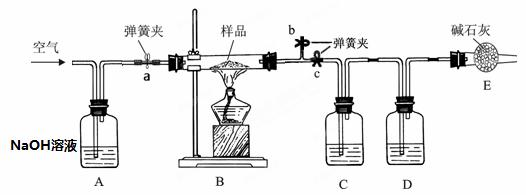
 对人体有害
对人体有害