题目内容
19.下列物质用途与性质对应关系合理的是CA.二氧化碳用于灭火--能与水反应 B.一氧化碳用于冶炼金属--氧化性
C.金刚石用于裁玻璃--硬度大 D.洗涤剂用于去除油污--乳化功能.
分析 A、根据二氧化碳的性质与用途进行分析判断.
B、根据一氧化碳具有还原性,进行分析判断.
C、根据金刚石是天然存在的最硬的物质,进行分析判断.
D、洗涤剂用于去除油污是乳化功能.
解答 解:A、二氧化碳用于灭火,是利用了二氧化碳不能燃烧、不能支持燃烧、密度比空气大的性质,故选项说法错误.
B、一氧化碳用于冶炼金属,是利用了一氧化碳的还原性,故选项说法错误.
C、金刚石是天然存在的最硬的物质,可用于裁玻璃,故选项说法正确.
D、洗涤剂用于去除油污是乳化功能.
故答案为:C;乳化功能
点评 本题难度不大,物质的性质决定物质的用途,掌握常见碳单质和氧化物的性质和用途是正确解答此类题的关键.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
11.下列属于氧化物的是( )
| A. | H2SO4 | B. | SO2 | C. | KOH | D. | O2 |
8.下列饮品属于溶液的是( )
| A. | 碘酒 | B. | 牛奶 | C. | 果粒橙 | D. | 豆浆 |

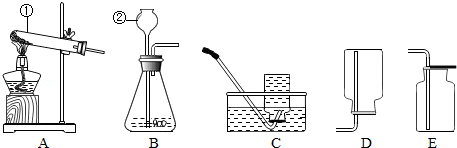
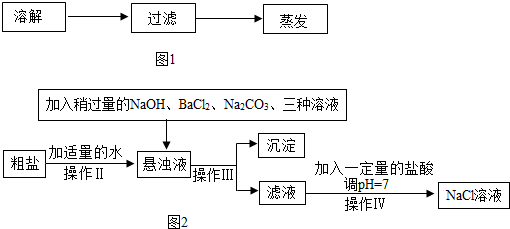
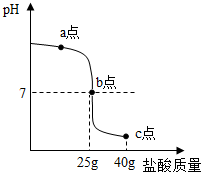 利用中和反应可以测定酸或碱溶液中溶质的质量分数.向20g溶质质量分数为4%的氢氧化钠溶液中不断滴加40g稀盐酸.
利用中和反应可以测定酸或碱溶液中溶质的质量分数.向20g溶质质量分数为4%的氢氧化钠溶液中不断滴加40g稀盐酸.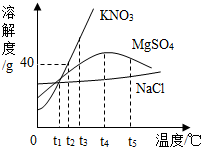 图中表示NaCl、KNO3、MgSO4三种物质的溶解度曲线.请回答:
图中表示NaCl、KNO3、MgSO4三种物质的溶解度曲线.请回答: