题目内容
3.镁在空气中燃烧生成氧化镁和氮化镁(其中氮为-3价),氮化镁与水反应生成氢氧化镁和氨气.(1)写出镁与空气中氮气化合成氮化镁的方程式3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2.
(2)写出氮化镁与水反应的化学方程式Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑.
(3)已知氮化镁是一种黄绿色的固体.根据镁在空气中燃烧的实验现象,可知在这样的条件下,镁更易与空气中的氧气化合,理由是镁在空气中燃烧生成白色固体.
分析 根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式.
解答 解:(1)镁与空气中氮气化合成氮化镁的方程式为:3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2;
(2)写出氮化镁与水反应的化学方程式为:Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑;
(3)已知氮化镁是一种黄绿色的固体,根据镁在空气中燃烧的实验现象,可知在这样的条件下,镁更易与空气中的氧气化合,理由是镁在空气中燃烧生成白色固体.
故填:3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2;Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑;氧气;镁在空气中燃烧生成白色固体.
点评 书写化学方程式要注意四步:一是反应物和生成物的化学式要正确;二是要遵循质量守恒定律,即配平;三是要有必要的条件;四是看是否需要“↑”或“↓”.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
11.对下列物质在氧气中燃烧的实验现象描述正确的是( )
| A. | 石蜡在氧气中燃烧时,有水和二氧化碳生成 | |
| B. | 硫在氧气中燃烧时,火焰呈蓝紫色,生成无气味的气体 | |
| C. | 红磷在氧气中燃烧时,生成一种红色固体 | |
| D. | 铝箔在氧气中燃烧时,发出耀眼的白光,生成白色固体 |
8.下列叙述正确的是( )
| A. | 原子是化学变化中的最小微粒 | |
| B. | 分子大,原子小 | |
| C. | 决定原子质量大小的主要是质子和电子 | |
| D. | 原子得到电子变成阳离子 |
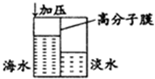 2015年4月29日,全国水资源管理工作座谈会在北京召开.
2015年4月29日,全国水资源管理工作座谈会在北京召开.