题目内容
配制50g质量分数为20%的食盐溶液,现提供25g质量分数为40%的食盐溶液、20g质量分数为15%的食盐溶液及足够多的固体食盐和水,设计二种方案并写出计算过程.
考点:一定溶质质量分数的溶液的配制
专题:溶液、浊液与溶解度
分析:根据所需配制的溶液计算出配制时所需要溶质和溶剂的质量,然后利用所提供的药品设计不同的配制所需溶液的方法.
解答:解:配制50g质量分数为20%的食盐溶液需要食盐的质量=50g×20%=10g,则需要水的质量=50g-10g=40g(合40mL);
可以直接称10g食盐、量取40mL水,混合溶解所得溶液即为所需配制的溶液;
可取40%的溶液加水稀释进行配制,需要40%的溶液的质量=10g÷40%=25g,加水的量=50g-25g(合25mL).
故答案为:方案一:10gNaCl溶液,40mL水;方案二:25g40%NaCl溶液,25mL水.
可以直接称10g食盐、量取40mL水,混合溶解所得溶液即为所需配制的溶液;
可取40%的溶液加水稀释进行配制,需要40%的溶液的质量=10g÷40%=25g,加水的量=50g-25g(合25mL).
故答案为:方案一:10gNaCl溶液,40mL水;方案二:25g40%NaCl溶液,25mL水.
点评:解决本题抓住关键点:配制需要10g食盐和40g水,只要设法满足这一要求,所设计的方案就是可行的.

练习册系列答案
相关题目
在pH=1的无色透明液体中,能大量共存的离子组合是( )
| A、Al3+,Ag+,NO3-,Cl- |
| B、Mg2+,NH4+,NO3-,Cl- |
| C、Ca2+,Cl-,NO3-,SO42- |
| D、Ca2+,OH-,Cl-,Na+ |
下列符号只表示微观意义的是( )
| A、Cl2 |
| B、2H2 |
| C、Cu |
| D、CO2 |
某同学欲配制50克质量分数为7.0%的食盐溶液,在量取水时,俯视读数,其他各步操作均正确,那么他实际上所配制的食盐水的质量分数( )
| A、>7.0% | B、<7.0% |
| C、=7.0% | D、无法判断 |
下列图象能正确反映对应变化关系的是( )
A、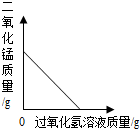 向一定量的二氧化锰中加入过氧化氢溶液 向一定量的二氧化锰中加入过氧化氢溶液 |
B、 加热一定量的高锰酸钾固体 加热一定量的高锰酸钾固体 |
C、 加热一定量的氯酸钾和二氧化锰的混合物 加热一定量的氯酸钾和二氧化锰的混合物 |
D、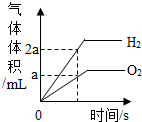 将一定质量水通电电解一段时间 将一定质量水通电电解一段时间 |