题目内容
7.除去下列物质中混有的杂质,所选用的试剂或操作方法不正确的是( )| 物质 | 杂质 | 除杂质选用的试剂和操作方法 | |
| A | CO2 | CO | 通过灼热的氧化铜 |
| B | 二氧化碳 | 氯化氢气体 | 通过氢氧化钠溶液 |
| C | Cu(NO3)2溶液 | AgNO3溶液 | 加入过量的铜粉,过滤 |
| D | 碳酸钙 | 氯化钙 | 加入足量的水溶解,过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、CO能与灼热的氧化铜反应生成铜和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
B、CO2和HCl气体均能与NaOH溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
C、过量的铜粉能与AgNO3溶液反应生成硝酸铜溶液和银,再过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
D、氯化钙易溶于水,碳酸钙难溶于水,可采取加水溶解、过滤、洗涤、干燥的方法进行分离除杂,故选项所采取的方法正确.
故选:B.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
7.分析推理是化学学习中常用的思维方法.下列分析推理正确的是( )
| A. | 金刚石很硬,故石墨也很硬 | |
| B. | 空气中二氧化硫会造成酸雨,所以空气中二氧化碳一定会造成酸雨 | |
| C. | 离子是带电荷的微粒,所以带电荷的微粒一定是离子 | |
| D. | 同温下分解氯酸钾,加催化剂的反应速率快,故催化剂可以改变反应速率 |
18.类推是常用的思维方法,以下类推正确的是( )
| A. | 酸溶液能使紫色石蕊变红,则能使紫色石蕊试液变红的一定是酸溶液 | |
| B. | 碱都含有氢元素和氧元素,所以含有氢元素和氧元素的物质一定是碱 | |
| C. | 酸雨的pH小于7,所以pH小于7的雨水是酸雨 | |
| D. | 二氧化碳可与氢氧化钠反应生成盐和水,则二氧化碳也可与氢氧化钙反应生成盐和水 |
2.夏天到了,衣服上常会留下难以淸洗的汗渍,果汁渍等.校“我与化学”兴趣小组对“污渍炸盐”(一种新型衣物助洗剂)化学成分进行探究,主要探究过程如下:
(1)阅读产品标签:“主要成分是过氧碳酸钠,能在瞬间去除洗衣粉难以除去的多重顽固污渍…,本产品不
不伤衣物,‘无磷’是它的一大优点”,含磷洗涤剂对环境的危害是导致江河湖泊及近海海域越来越频繁的水华和赤潮现象,造成水质恶化.
(2)查阅资料:过氧碳酸钠(Na2CO4),白色结晶颗粒,其溶于水会产生碳酸盐和其他化合物;
(3)合理猜想:①其化合物为NaOH;②其化合物为H202;@其化合均为NaOH和H2O2;该小组同学做出以上猜想的理论依据是质量守恒定律,化学反应前后元素的种类和质量不变.
(4)实验设计:探究“污灌爆炸盐”水溶液的成份,完成下列表格.
限选试剂:稀盐酸、BaCl2溶液、MgCl2溶液、MnO2、蒸馏水
(1)阅读产品标签:“主要成分是过氧碳酸钠,能在瞬间去除洗衣粉难以除去的多重顽固污渍…,本产品不
不伤衣物,‘无磷’是它的一大优点”,含磷洗涤剂对环境的危害是导致江河湖泊及近海海域越来越频繁的水华和赤潮现象,造成水质恶化.
(2)查阅资料:过氧碳酸钠(Na2CO4),白色结晶颗粒,其溶于水会产生碳酸盐和其他化合物;
(3)合理猜想:①其化合物为NaOH;②其化合物为H202;@其化合均为NaOH和H2O2;该小组同学做出以上猜想的理论依据是质量守恒定律,化学反应前后元素的种类和质量不变.
(4)实验设计:探究“污灌爆炸盐”水溶液的成份,完成下列表格.
限选试剂:稀盐酸、BaCl2溶液、MgCl2溶液、MnO2、蒸馏水
| 实验步驟 | 实验现象 | 实验结论 |
| 步骤1:取少量“污清爆炸盐”于烧杯中,加入足量蒸馏水,充分搅拌 | 固体完全溶解,形成无色溶液 | \ |
| 步驟2:取少量步驟1形成的溶液与试管中,再滴加稀盐酸,振荡,静置 | 有气泡产生 | 含有Na2CO3 |
| 步骤3:取少置步骤2试管中的上层清液与另一支试管中,再滴加少量MgCl2溶液,振荡. | 无明显现象 | 不含NaOH |
| 步骤4:另取一支试管,加入少量步骤1形成的溶液,再加入MnO2,将带火星木条伸入试管中. | 带火星木条复燃 | 含有H2O2 |
12.腈纶和羊毛常用于制作服装面料,区分腈纶和羊毛的最可靠方法是( )
| A. | 闻气味 | B. | 用手触摸 | C. | 灼烧 | D. | 用水浸泡 |
17.下列化学方程式和事实相符并书写正确的是( )
| A. | 实验室检验二氧化碳:2NaOH+CO2═H2O+Na2CO3 | |
| B. | 双氧水分解制取氧气:H2O2$\frac{\underline{\;MnO_2\;}}{\;}$H2↑+O2↑ | |
| C. | 实验室制氢气:Zn+H2SO4═H2↑+ZnSO4 | |
| D. | 铁溶于稀盐酸:2Fe+6HCl═2FeCl3+3H2↑ |
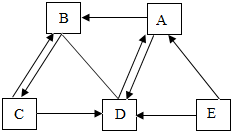 A、B、C、D、E是初中化学常见的物质.A为盐,C为单质;生活中B和D都可用来灭火;E广泛用于玻璃、造纸、纺织、洗涤剂的生产.它们之间的一部分关系如图所示,(图中“-表示两端的物质能发生化学反应”;“→”表示物质间存在转化关系.部分反应物或生成物已略去)
A、B、C、D、E是初中化学常见的物质.A为盐,C为单质;生活中B和D都可用来灭火;E广泛用于玻璃、造纸、纺织、洗涤剂的生产.它们之间的一部分关系如图所示,(图中“-表示两端的物质能发生化学反应”;“→”表示物质间存在转化关系.部分反应物或生成物已略去)