题目内容
6.测定空气中氧气含量实验,红磷燃烧集气瓶内放水的作用是尽快降低集气瓶内的温度.分析 根据水能够吸收红磷燃烧放出的热量,从而降低集气瓶内的温度分析.
解答 集气瓶内的水能够吸收反应放出的热,可以使集气瓶内的温度尽快降低到室温.
故填:尽快降低集气瓶内的温度.
点评 本题考查了氧气含量的测定,结合集气瓶内的水考查了水的作用,注意水在不同的环境中有不同的用途,能够考查学生的分析能力.

练习册系列答案
相关题目
17.如图所示的实验操作正确的是( )
| A. | 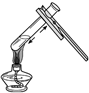 加热液体 | B. | 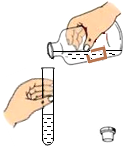 倾倒药品 | C. | 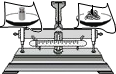 称量药品 | D. | 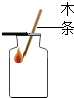 CO2的验满 |
14.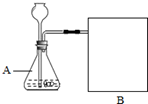 某研究性学习小组,选择“过氧化氢(H202)生成氧气(02)的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程.
某研究性学习小组,选择“过氧化氢(H202)生成氧气(02)的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程.
【假设】过氧化氢生成氧气的快慢与催化剂的种类有关.
实验方案】常温下,在两瓶相同体积的过氧化氢(H202)溶液中分别加入相同质量的二氧化锰(MnO2)和红砖粉,测量各生成一瓶(相同体积)氧气所需的时间.
【进行实验】上图是他们进行实验的装置图,气体发生装置中A仪器的名称是锥形瓶,此实验中B处宜采用的气体收集方法是排水法.
【实验记录】
【结论】该探究过程得出的结论是H2O2生成氧气的快慢与催化剂种类有关;故填:H2O2生成氧气的快慢与催化剂种类有关
【反思】过氧化氢在常温下分解缓慢,加入二氧化锰或红砖粉后反应明显加快,若要证明二氧化锰(MnO2)和红砖粉是该反应的催化剂,还需增加实验来验证它们在化学反应前后的质量 和化学性质 是否改变.
 某研究性学习小组,选择“过氧化氢(H202)生成氧气(02)的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程.
某研究性学习小组,选择“过氧化氢(H202)生成氧气(02)的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程.【假设】过氧化氢生成氧气的快慢与催化剂的种类有关.
实验方案】常温下,在两瓶相同体积的过氧化氢(H202)溶液中分别加入相同质量的二氧化锰(MnO2)和红砖粉,测量各生成一瓶(相同体积)氧气所需的时间.
【进行实验】上图是他们进行实验的装置图,气体发生装置中A仪器的名称是锥形瓶,此实验中B处宜采用的气体收集方法是排水法.
【实验记录】
| 实验编号 | 1 | 2 |
| 反应物 | 6%过氧化氢(H202) | 6%过氧化氢(H202) |
| 催化剂 | 1g 二氧化锰 | |
| 时间 | 35s | 152s |
【反思】过氧化氢在常温下分解缓慢,加入二氧化锰或红砖粉后反应明显加快,若要证明二氧化锰(MnO2)和红砖粉是该反应的催化剂,还需增加实验来验证它们在化学反应前后的质量 和化学性质 是否改变.
16.小明同学在做家庭实验时,不小心将过氧化氢溶液溅到妈妈刚刚切好的土豆丝上,发现土豆丝上立即冒气泡,激发了小明的探究欲望,请你参与小明的探究.
【猜想】土豆丝可作过氧化氢分解的催化剂
【实验】设计并完成下表所示的探究实验:
(1)请你帮小明同学填写上表中未填完的空格.
(2)在小明的探究实验中,“实验一”和“实验二”起的作用是对比或对照
【反思】小凡同学认为仅由上述实验还不能完全得出表内的“总结”,他补充设计了两个方面的探究实验.
第一方面探究土豆丝在化学反应前后化学性质是否改变.
向反应后试管内的剩余物中重新加入过氧化氢溶液,有大量气泡产生,且木条复燃;
第二方面探究土豆丝在化学反应前后质量是否改变.
实验操作中包含了两次称量,将实验二试管中的物质进行过滤、洗涤、干燥、称量(土豆丝本身的水分减少忽略不计).
【猜想】土豆丝可作过氧化氢分解的催化剂
【实验】设计并完成下表所示的探究实验:
| 实验操作 | 实验现象 | 结论 | 总结 | |
| 实验一 | 取5mL5%的过氧化氢溶液于试管中,伸入带火星木条 | 有小气泡产生,木条不复燃 | 过氧化氢分解产生氧气,但是 速率慢 | 土豆丝可作过氧化氢分解的催化剂 |
| 实验二 | 取5mL5%的过氧化氢溶液于试管中,加入土豆丝,伸入带火星木条 | 迅速产生大量气泡, 木条复燃 | 土豆丝能加快过氧化氢的分解的速率 |
(2)在小明的探究实验中,“实验一”和“实验二”起的作用是对比或对照
【反思】小凡同学认为仅由上述实验还不能完全得出表内的“总结”,他补充设计了两个方面的探究实验.
第一方面探究土豆丝在化学反应前后化学性质是否改变.
向反应后试管内的剩余物中重新加入过氧化氢溶液,有大量气泡产生,且木条复燃;
第二方面探究土豆丝在化学反应前后质量是否改变.
实验操作中包含了两次称量,将实验二试管中的物质进行过滤、洗涤、干燥、称量(土豆丝本身的水分减少忽略不计).

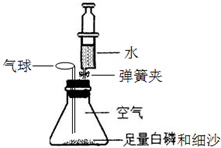 某实验小组利用如图所示装置测定空气中氧气体积分数并取得成功.
某实验小组利用如图所示装置测定空气中氧气体积分数并取得成功.