题目内容
为了测定某产品中碳酸钡的质量分数进行了如下实验。取一定量的样品和400g溶质质量分数为10%的稀盐酸放入烧杯中。在化学反应过程中对烧杯及其中的剩余物进行了五次称量,记录如下表:(假设反应匀速进行;杂质不溶于水,也不与稀盐酸反应,烧杯的质量为25.4g)
| 反应时间 | t1 | t2 | t3 | t4 | t5 |
| 烧杯和药品质量/g | 516.6 | 507.8 | m | 503.4 | 503.4 |
请计算:(反应方程式为:BaCO3 + 2HCl = BaCl2 + H2O + CO2↑)
(1)表中的“m”为。
(2)该产品中碳酸钡的质量分数。
(3)当产品中碳酸钡与稀盐酸恰好完全反应时,所得溶液中溶质的质量分数。
(1)503.4g
(2)516.6g-507.8g=8.8g, 507.8g-503.4g=4.4g, 8.8g+8.8g+4.4g=22g
解:设碳酸钡的质量为x,消耗盐酸的质量为y,产生氯化钡的质量为z。
BaCO3 + 2HCl = BaCl2 + H2O + CO2↑
 197 73 208 44
197 73 208 44
x y z 22g
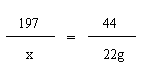 | |||
|

 初中学业考试导与练系列答案
初中学业考试导与练系列答案下列实验操作中,现象足以说明结论的是
| 操 作 | 现 象 | 结 论 | |
| A | 在混有碳酸钠的氢氧化钠溶液样品中,加入氢氧化钙溶液,过滤 | 出现白色沉淀 | 碳酸钠已被除净 |
| B | 将浓盐酸和大理石反应放出的气体通入澄清石灰水 | 石灰水未变 浑浊 | 该石灰水一定变质 |
| C | 向滴有酚酞的氢氧化钠溶液的试管中滴加一定量的稀盐酸 | 红色褪去 | 说明氢氧化钠与盐酸发生了化学反应 |
| D | 将充满二氧化碳气体的试管倒扣在盛有氢氧化钠溶液的水槽中 | 试管内液面 上升 | 二氧化碳与氢氧化钠一定发生了反应 |
 A的无色溶液,滴加石蕊试液,溶液呈蓝色。A的水溶液显性。
A的无色溶液,滴加石蕊试液,溶液呈蓝色。A的水溶液显性。