题目内容
14.有一包粉末,可能由NaCl、Na2CO3、FeCl3、MgCl2中的一种或几种组成,现做如下实验:①取少量粉末,加水溶解,得无色透明溶液;
②取①中所得溶液少许,加入氢氧化钠溶液,无明显现象;
③另取少量粉末,滴加稀盐酸,有气泡产生.
(1)由实验①可知,原粉末中不含氯化铁;
(2)由实验②可知,原粉末中不含氯化镁;
(3)由实验③可知,原粉末中含有碳酸钠;
(4)根据上述实验,可知原粉末中可能含有碳酸钠或碳酸钠、氯化钠.
分析 根据氯化铁在溶液中显黄色,氯化镁和氢氧化钠会生成氢氧化镁沉淀,碳酸钠和盐酸会生成二氧化碳气体等知识进行分析.
解答 解:氯化铁在溶液中显黄色,氯化镁和氢氧化钠会生成氢氧化镁沉淀,碳酸钠和盐酸会生成二氧化碳气体.
(1)由实验①可知,取少量粉末,加水溶解,得无色透明溶液,氯化铁在溶液中显黄色,所以原粉末中不含氯化铁;
(2)由实验②可知,取①中所得溶液少许,加入氢氧化钠溶液,无明显现象,氯化镁和氢氧化钠会生成氢氧化镁沉淀,所以原粉末中不含氯化镁;
(3)由实验③可知,另取少量粉末,滴加稀盐酸,有气泡产生,碳酸钠和盐酸会生成二氧化碳气体,所以原粉末中含有碳酸钠;
(4)题中的现象不能确定是否含有氯化钠,所以原粉末中可能含有碳酸钠或碳酸钠、氯化钠.
故答案为:(1)不含氯化铁;
(2)不含氯化镁;
(3)含有碳酸钠;
(4)碳酸钠或碳酸钠、氯化钠.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

练习册系列答案
相关题目
4.某同学梳理并归纳了以下知识点:①用肥皂水能区分硬水和软水;②在化学反应中只有燃烧才能放出热量;③农业上可以用二氧化碳做气体肥料;④最外层电子数为8的粒子一定是稀有气体的原子;⑤无论是吸入的空气还是呼出的气体中含量最多的气体都是氧气;⑥爱护水资源的有效途径是防止水体污染等.其中正确的是( )
| A. | ①②④ | B. | ①③④ | C. | ①③⑥ | D. | ②⑤⑥ |
19.某反应的微观示意图如图(一种小球代表一种元素的原子),下列说法错误的是( )
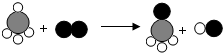

| A. | 该反应是置换反应 | B. | 该反应的本质是原子的重新组合 | ||
| C. | 该反应前后分子的种类改变 | D. | 该反应中的生成物都是化合物 |
 某补钙药剂的标签主要内容如图所示,为测定该钙片含量是否符合标注,做如下实验:取10片该钙片粉碎,放人干燥、洁净的烧杯中,再向烧杯中加入50g稀盐酸,恰好完全反应(钙片中其他成分不溶于水,也不和稀盐酸反应,反应中产生的气体全部放出),反应后称量烧杯内剩余物质的总质量为64.5g.
某补钙药剂的标签主要内容如图所示,为测定该钙片含量是否符合标注,做如下实验:取10片该钙片粉碎,放人干燥、洁净的烧杯中,再向烧杯中加入50g稀盐酸,恰好完全反应(钙片中其他成分不溶于水,也不和稀盐酸反应,反应中产生的气体全部放出),反应后称量烧杯内剩余物质的总质量为64.5g.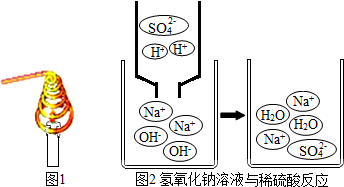
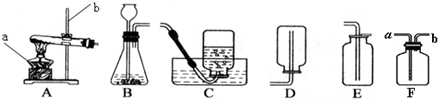
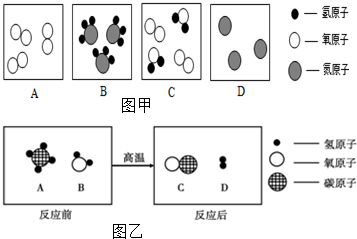 在宏观、微观和符号之间建立联系是化学学科的特点.
在宏观、微观和符号之间建立联系是化学学科的特点.