题目内容
13.工业上用废铁制取铁红(氧化铁)的简要流程图如下(杂质不与酸反应,也不溶于水)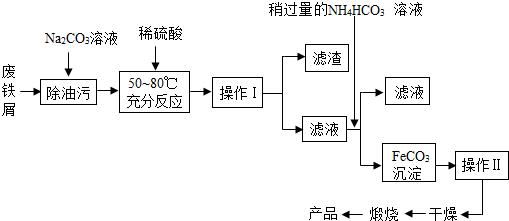
(1)操作Ⅰ的名称是过滤,该操作用到玻璃棒,其作用是引流.
(2)写出上述变化流程中的一种氧化物的化学式Fe2O3.
(3)在加入稀硫酸的操作步骤中,如何判断已经充分反应了?没有气泡产生,写出该处的一个化学反应方程式Fe+H2SO4=FeSO4+H2↑.
分析 (1)根据操作Ⅰ的分离过程来分析;
(2)根据氧化物的概念来分析;
(3)铁与稀硫酸反应生成硫酸亚铁和氢气.
解答 解:(1)操作Ⅰ是分离开了滤渣和滤液,则为过滤,其中玻璃棒的作用是引流;故填:过滤;引流;
(2)最终的产品铁红即为氧化铁,是一种由两种元素组成,且有一种元素为氧元素的化合物,属于氧化物,故填:Fe2O3;
(3)铁与稀硫酸反应生成硫酸亚铁和氢气,故看到没有气泡产生说明已经充分反应,故填:没有气泡产生;Fe+H2SO4=FeSO4+H2↑.
点评 本题是一道框图推断题,考查知识面较广,要求学生具有分析和解决问题的能力,难度较大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.下列各组物质只用水这一种试剂进行相关操作不能达到目的是( )
| A. | 提纯混有氧化钙的碳酸钙 | B. | 除去氧化钙中混有的碳酸钙 | ||
| C. | 鉴别氢氧化钠和硝酸铵固体 | D. | 分离硝酸钾和氯化钠固体 |
4.下列说法中正确的是( )
| A. | 白色污染就是白色建筑垃圾的污染 | |
| B. | 用氢氧化钠去污是因为氢氧化钠能乳化油污 | |
| C. | 75%的医用酒精中,C2H5OH与H2O的质量比为3:1 | |
| D. | 在树木上涂刷含有硫磺粉等的石灰浆,可以保护树木防止害虫生卵 |
1.要除去NaNO3溶液中含有少量的NaCl和BaCl2杂质,得到纯净的NaNO3,应依次加入( )
| A. | K2CO3溶液、AgNO3溶液 | B. | AgNO3溶液、稀H2SO4 | ||
| C. | 稀H2SO4、AgNO3溶液 | D. | AgNO3溶液、Na2SO4溶液 |