题目内容
19.20℃时,将40gNaCl放入100g水中,搅拌后,所得溶液中NaCl的质量分数是(已知20℃时,NaCl的溶解度为36g)( )| A. | $\frac{40}{100}$×100% | B. | $\frac{40}{100+40}$×100% | C. | $\frac{36}{100}$×100% | D. | $\frac{36}{100+36}$×100% |
分析 由20℃时NaCl在水中的溶解度是36g,判断100g水中最多能够溶解36gNaCl;利用饱和溶液的溶质质量分数与溶解度的关系,计算溶液的溶质质量分数.
解答 解:由20℃时NaCl在水中的溶解度是36g,判断100g水中最多能够溶解36gNaCl,所以加入40g氯化钠不能完全溶解,即得饱和溶液,故其溶液中溶质的质量分数为:$\frac{36g}{36g+100g}$×100%
故选D.
点评 某温度下的溶解度即该温度下100g水所能溶解该溶质质量的最大值,因此利用物质的溶解度可判断一定量溶剂中溶解一定溶质后所得溶液是否达到饱和.

练习册系列答案
相关题目
4.在一密闭容器内有四种物质在一定条件下充分反应,测得反应前后各物质的质量如下:
(1)反应后D的质量X为9;
(2)参加反应的物质是A和D.反应生成的物质质量比是1:7.
| 物质 | A | B | C | D |
| 反应前质量/g | 4 | 10 | 1 | 21 |
| 反应后质量/g | 0 | 12 | 15 | X |
(2)参加反应的物质是A和D.反应生成的物质质量比是1:7.
10.要取用7mL的盐酸,可选用( )规格的量筒.
| A. | 10 mL | B. | 20 mL | C. | 50 mL | D. | 100 mL |
4.下列对分子、原子、离子的认识正确的是( )
| A. | 温度越高,分子运动速率越快 | |
| B. | 原子是最小的粒子,不可再分 | |
| C. | 离子不能直接构成物质 | |
| D. | 固体难压缩,说明固体分子间无间隔 |
11.淮安是一座美丽的水城,水在人们生产、生活中起着重要作用.下列说法错误的是( )
| A. | 收集雨水用于城市绿化用水 | B. | 过滤可除去水中所有物质 | ||
| C. | 生活中常用肥皂水区分硬水和软水 | D. | 可用沉降、过滤、吸附等方法净化水 |
8.化学实验既要操作规范,更要保障安全,下列实验操作不符合这一要求的是( )
| A. | 做铁丝在氧气中燃烧实验,集气瓶底部要预先加少量水 | |
| B. | 用酒精灯外焰给试管中固体物质加热时,试管口要略向下倾斜 | |
| C. | 加热高锰酸钾制氧气,试管口要放一团蓬松的棉花 | |
| D. | 试验结束时,剩余的药品都要及时放回原瓶 |
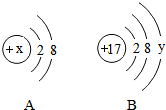 化学用语是最简明、信息丰富、国际通用的语言.
化学用语是最简明、信息丰富、国际通用的语言.