题目内容
8. 右图是测定空气中氧气含量的装置,请回答下列问题:
右图是测定空气中氧气含量的装置,请回答下列问题:(1)点燃燃烧匙中的红磷,迅速插入集气瓶中,观察到现象为:红磷继续燃烧并产生大量白烟.
该反应的文字表达式为磷+氧气$\stackrel{点燃}{→}$五氧化二磷.
(2)冷却后,打开止水夹,可观察到的现象是烧杯中的水进入集气瓶,集气瓶内水面上升,说明氧气约占空气总体积的$\frac{1}{5}$
(3)瓶内剩余的气体主要是氮气,由该实验可得出该气体难(填“易”或“难”)溶于水和化学性质不活泼(填“活泼”或“不活泼”)的结论.
(4)实验过程中,燃烧匙内盛放过量的红磷的目的是将瓶内的空气中的氧气全部消耗.
分析 (1)根据红磷燃烧的现象和反应的原理解答;
(2)根据红磷测定空气组成的实验原理、操作、现象、结论和注意事项,并结合空气的成分及其体积分数等,解答本题;
(3)集气瓶内剩余的气体主要是氮气,说明氮气不支持燃烧,化学性质不活泼;集气瓶内剩余的气体主要是氮气,说明氮气难溶于水;
(4)根据该实验的原理:红磷燃烧消耗氧气生成固体,进入的水占居瓶中空气中原来氧气的体积分析解答.
解答 解:(1)将燃着的红磷立即伸入盛有少量水的集气瓶中,红磷继续燃烧并产生大量白烟,一会熄灭,红磷与氧气反应生成五氧化二磷,反应的文字表达式为:磷+氧气$\stackrel{点燃}{→}$五氧化二磷;故答案为:红磷继续燃烧并产生大量白烟;磷+氧气$\stackrel{点燃}{→}$五氧化二磷;
(2)待红磷熄灭并冷却后,打开弹簧夹,由于集气瓶内的氧气被消耗,瓶内气体压强减小,故烧杯内的水沿导管进入集气瓶,进入水的体积约占空气体积的五分之一,故答案为:烧杯中的水进入集气瓶,集气瓶内水面上升,约占空气体积的$\frac{1}{5}$;
(3)根据空气的主要成分是氮气和氧气,可知瓶内剩余的气体主要是氮气.由该实验的现象(水并没有充满整个集气瓶;过量的红磷不能在其中继续燃烧),可推断得出氮气难溶于水和化学性质不活泼的结论.故答案:氮气;难;不活泼;
(4)实验过程中,燃烧匙内盛放过量的红磷的目的是:将瓶内的空气中的氧气全部消耗;故答案:将瓶内的空气中的氧气全部消耗.
点评 本题主要考查用红磷测定空气组成的实验原理、操作、现象、结论和注意事项,难度稍大.

练习册系列答案
 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
19.正确的化学实验操作对实验结果、人身安全非常重要.下图中的实验操作正确的是( )
| A. | 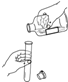 倾倒液体 | B. | 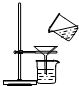 过滤 | C. | 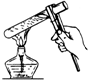 给液体加热 | D. | 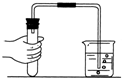 检查装置气密性 |
3.最近我国爆发了三鹿婴幼儿奶粉受污染事件,九月份生产的11批次的三鹿牌婴幼儿奶粉中检出了含量不同的三聚氰胺.三聚氰胺是一种低毒性化工产品,婴幼儿大量摄入会引起泌尿系统疾患.下列描述属于三聚氰胺的化学性质的是( )
| A. | 加热升华,升华温度300℃ | |
| B. | 在一般情况下较稳定,但在高温下可能会分解放出氰化物 | |
| C. | 溶于热水,微溶于冷水,极微溶于热乙醇 | |
| D. | 三聚氰胺性状为纯白色单斜棱晶体,无味 |
20.一定质量含杂质的铁粉中(假设杂质不溶于水,也不与其他物质反应)加入l60g溶质的质量分数为l0%的硫酸铜溶液,恰好完全反应后,过滤得到6.8g干燥固体,则含杂质的铁的质量是( )
| A. | 6.0 g | B. | 5.6g | C. | 16g | D. | 6.4g |
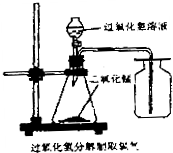 实验室常采用分解过氧化氢溶液(二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气.
实验室常采用分解过氧化氢溶液(二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气.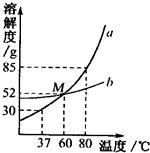 如图为a、b两物质的溶解度曲线,请依图回答下列问题:
如图为a、b两物质的溶解度曲线,请依图回答下列问题: