题目内容
2. 氨气(NH3)是一种极易溶于水的气体,氨气呈碱性,实验室常用氯化铵和熟石灰混合加热制取氨气,同时还生成氯化钙和水.请用化学方程式表示实验室制取氨气的化学反应原理,并描述如图中可观察到的现象.
氨气(NH3)是一种极易溶于水的气体,氨气呈碱性,实验室常用氯化铵和熟石灰混合加热制取氨气,同时还生成氯化钙和水.请用化学方程式表示实验室制取氨气的化学反应原理,并描述如图中可观察到的现象.
分析 根据已有的知识进行分析解答,氯化铵能与氢氧化钙加热反应生成氯化钙、水和氨气,根据氨气与水的反应以及溶液的酸碱性进行分析解答即可.
解答 解:氯化铵能与氢氧化钙加热反应生成氯化钙、水和氨气,氨气极易溶于水,导致试管内的压强变小,水会沿试管上升;氨气的水溶液呈碱性,能使酚酞试液变红,故答案为:Ca(OH)2+2NH4Cl $\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;试管内的液面上升,进入试管的水呈红色.
点评 本题考查的是化学方程式的书写以及物质反应与物理压强知识的结合,完成此题,可以依据已有的知识进行.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目
12.化学兴趣小组欲探究自己使用的某品牌牙膏的主要成分.
【查阅资料】
(1)牙膏的成分有活性物质、摩擦剂、保持牙膏湿润的甘油等物质.
(2)常用的牙膏摩擦剂的主要成分有CaCO3、Al(OH)3、SiO2.
(3)牙膏除了碳酸钙以外,其他物质均不与稀盐酸反应产生气体.
(4)SiO2不溶于水,也不与盐酸反应.Al(OH)3和氢氧化钠溶液反应生成偏铝酸钠(NaAlO2)和水,该反应的化学方程式为Al(OH)3+NaOH=NaAlO2+2H2O.偏铝酸钠和适量稀盐酸反应生成氢氧化铝,氢氧化铝和稀盐酸可以发生中和反应.
(5)相关物质的溶解性表:
该品牌牙膏含有上述摩擦剂中的两种成分,为探究摩擦剂的组成,化学兴趣小组取适量该牙膏加水充分搅拌、静置、过滤、洗涤、干燥,得到该牙膏中的摩擦剂.
【提出猜想】猜想1:摩擦剂的成分为Al(OH)3和CaCO3.
猜想2:摩擦剂的成分为SiO2和CaCO3.
猜想3:摩擦剂的成分为SiO2和Al(OH)3.
设计实验】
【实验结论】经过实验验证,猜想1成立.
【实验反思】同学们为进一步确认摩擦剂中含有氢氧化铝,先在少量牙膏样品中加入过量的氢氧化钠溶液,静置一段时间,取上层清液,再滴加稀盐酸至过量.整个实验过程中观察到的现象为牙膏样品中部分固体溶解,向上层清夜中滴加稀盐酸时开始无现象,之后有固体产生,最后固体溶解,依据该现象可以判断摩擦剂中一定含有氢氧化铝.
【查阅资料】
(1)牙膏的成分有活性物质、摩擦剂、保持牙膏湿润的甘油等物质.
(2)常用的牙膏摩擦剂的主要成分有CaCO3、Al(OH)3、SiO2.
(3)牙膏除了碳酸钙以外,其他物质均不与稀盐酸反应产生气体.
(4)SiO2不溶于水,也不与盐酸反应.Al(OH)3和氢氧化钠溶液反应生成偏铝酸钠(NaAlO2)和水,该反应的化学方程式为Al(OH)3+NaOH=NaAlO2+2H2O.偏铝酸钠和适量稀盐酸反应生成氢氧化铝,氢氧化铝和稀盐酸可以发生中和反应.
| 物质 | Al(OH)3 | NaAlO2 | AlCl3 |
| 溶解性 | 不溶 | 溶 | 溶 |
该品牌牙膏含有上述摩擦剂中的两种成分,为探究摩擦剂的组成,化学兴趣小组取适量该牙膏加水充分搅拌、静置、过滤、洗涤、干燥,得到该牙膏中的摩擦剂.
【提出猜想】猜想1:摩擦剂的成分为Al(OH)3和CaCO3.
猜想2:摩擦剂的成分为SiO2和CaCO3.
猜想3:摩擦剂的成分为SiO2和Al(OH)3.
设计实验】
| 实验步骤 | 预期实验现象 | 预期实验结论 |
组装下图装置进行实验.取少量摩擦剂于锥形瓶中,加入适量的稀盐酸.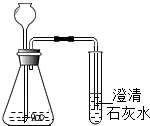 | 固体全部溶解,有气泡,石灰水变混浊 | 则猜想1成立 锥形瓶中发生的化学反应方程式为Al(OH)3+3HCl=AlCl3+3H2O CaCO3+2HCl=CaCl2+H2O+CO2↑ |
| 摩擦剂部分溶解 石灰水无明显变化 | 则猜想3成立 |
【实验反思】同学们为进一步确认摩擦剂中含有氢氧化铝,先在少量牙膏样品中加入过量的氢氧化钠溶液,静置一段时间,取上层清液,再滴加稀盐酸至过量.整个实验过程中观察到的现象为牙膏样品中部分固体溶解,向上层清夜中滴加稀盐酸时开始无现象,之后有固体产生,最后固体溶解,依据该现象可以判断摩擦剂中一定含有氢氧化铝.
13.下列叙述中没有化学变化的是( )
| A. | 蜡烛燃烧 | B. | 钢铁锈蚀 | C. | 呼吸作用 | D. | 干冰升华 |
17.“绿色化学”要求原料物质中所有的原子完全被利用,全部转入期望的产品中,即原子利用率为100%,由C2H4(乙烯)合成C4H8O2(乙酸乙酯)的过程中,为使原子利用率达到100%,在催化剂作用下还需加入的物质是( )
| A. | CH3COOH | B. | H2O和CO2 | C. | O2和H2O | D. | CO2 |
2.1996年诺贝尔化学奖授予对发现发现C60有重大贡献的三位科学家,现在C70也已制的.以下对C60和C70这两种物质的叙述中错误的是( )
| A. | 它们是两种新型的化合物 | B. | 它们是由碳元素形成的两种单质 | ||
| C. | 它们的化学性质是完全相同的 | D. | 它们的相对分子质量相差为120 |
 一天,实验助手小林走进实验室,和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”(如图).
一天,实验助手小林走进实验室,和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”(如图).