题目内容
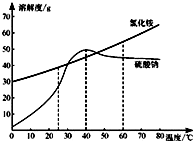 如图为氯化铵和硫酸钠的溶解度曲线.请回答:
如图为氯化铵和硫酸钠的溶解度曲线.请回答:(1)40℃时硫酸钠的溶解度比氯化铵的溶解度
(2)要把60℃氯化铵饱和溶液转化为不饱和溶液,可以采取的办法
(3)25℃时,向盛有200g水的小烧杯中加入100g氯化铵,搅拌,所得的溶液为
(4)90℃时,现有氯化铵和硫酸钠均恰好饱和的混合溶液,如果希望得到较纯净的氯化铵晶体,你的操作是:
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用,饱和溶液和不饱和溶液相互转变的方法
专题:溶液、浊液与溶解度
分析:根据固体物质的溶解度曲线可知:①比较不同物质在同一温度下的溶解度的大小,从而可以判断出形成的溶液中溶质的质量分数的大小,②判断物质的溶解度随温度变化的变化情况,从而可以确定出不饱和溶液和饱和溶液间的转化方法及分离混合物的方法等.
解答:解:(1)根据两物质的溶解度曲线可知,在40℃时,硫酸钠的溶解度大于氯化铵的溶解度,故答案为:大
(2)由于氯化铵的溶解度随温度的升高而增大,因此可以采用升温或增加溶剂的方法使它的饱和溶液变为不饱和溶液,故答案为:升温
(3)由于在25℃时,氯化铵的溶解度大约是40g,所以25℃时,向盛有200g水的小烧杯中加入100g氯化铵,搅拌,所得的溶液为饱和溶液;升温后溶液变为不饱和溶液,溶质质量分数=
×100%=33.3%;将上述溶液蒸发掉100g水后冷却到25时只能溶解40g,所以析出晶体60g.
(4)由于大于50℃时氯化铵溶解度随温度的升高而明显增大,而硫酸钠的溶解度随温度升高而减小,因此为除去氯化铵中少量硫酸钠时,应采取降温到50℃,再过滤、洗涤干燥.
故答案为:(1)大;(2)升温;(3)饱和;33.3%;60g;(4)降温到50℃.
(2)由于氯化铵的溶解度随温度的升高而增大,因此可以采用升温或增加溶剂的方法使它的饱和溶液变为不饱和溶液,故答案为:升温
(3)由于在25℃时,氯化铵的溶解度大约是40g,所以25℃时,向盛有200g水的小烧杯中加入100g氯化铵,搅拌,所得的溶液为饱和溶液;升温后溶液变为不饱和溶液,溶质质量分数=
| 100g |
| 100g+200g |
(4)由于大于50℃时氯化铵溶解度随温度的升高而明显增大,而硫酸钠的溶解度随温度升高而减小,因此为除去氯化铵中少量硫酸钠时,应采取降温到50℃,再过滤、洗涤干燥.
故答案为:(1)大;(2)升温;(3)饱和;33.3%;60g;(4)降温到50℃.
点评:本题难度不是很大,主要考查了固体溶解度曲线的意义及其应用,从而培养学生分析问题、解决问题的能力.

练习册系列答案
相关题目
厨房中发生的下列变化,一定属于化学变化的是( )
| A、用活性炭除去冰箱中的异味 |
| B、壶中水沸腾 |
| C、石油液化气燃烧 |
| D、用油烟机将油烟排出室外 |
地壳中含量最多的金属元素和最多的非金属元素组成的化合物的化学式是( )
| A、Fe2O3 |
| B、SiO2 |
| C、Al2O3 |
| D、N2O5 |
根据钠原子结构示意图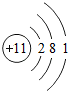 ,判断下列说法错误的是( )
,判断下列说法错误的是( )
 ,判断下列说法错误的是( )
,判断下列说法错误的是( )| A、钠原子核外有3个电子层 |
| B、钠原子在化学反应中容易得电子 |
| C、钠原子的质子数为11 |
| D、钠原子在化学反应中容易失电子 |
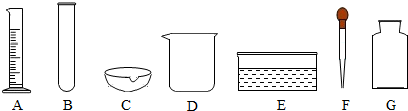

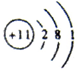 元素周期表是学习和研究化学的重要工具,它的内容十分丰富.下表是元素周期表的部分内容,请认真分析并回答后面的问题:
元素周期表是学习和研究化学的重要工具,它的内容十分丰富.下表是元素周期表的部分内容,请认真分析并回答后面的问题: