题目内容
11.某盐溶中滴入BaCl2溶液后,生成白色沉淀,再加稀HNO3,沉淀不溶解.则白色沉淀一定是BaSO4吗?该盐溶液一定是硫酸盐溶液吗?分析 根据已知条件“混入BaCl2溶液,产生白色沉淀”可知,生成的沉淀可能为为硫酸钡或氯化银,再滴入稀硝酸,沉淀不溶解,溶液中可能含有银离子或硫酸根离子进行分析.
解答 解:与氯化钡反应生成不溶于稀硝酸的白色沉淀,此沉淀可能是硫酸钡或氯化银,因此未知溶液中可能含有银离子或硫酸根离子,所以该盐溶液不一定是硫酸盐溶液.
故答案为:与氯化钡反应生成不溶于稀硝酸的白色沉淀,此沉淀可能是硫酸钡或氯化银,因此未知溶液中可能含有银离子或硫酸根离子,所以该盐溶液不一定是硫酸盐溶液.
点评 此题主要是考查同学们的综合分析能力,不但要求同学们具备有关化合物的基础知识,而且要有实验操作的经历和分析、解决化学实验问题的能力.解题时需要认真分析题目给出的条件,联系实际,逐一分析推断.

练习册系列答案
相关题目
2.小苏打和纯碱的日常生活中常用物质,某实验小组学习了相关知识后探究对比两种物质,进行了如下实验.
结合已学知识,回答下列问题.
(1)通过上述2个实验,可以得到的结论有(至少写出2点)碳酸氢钠受热会发生分解、碳酸氢钠与盐酸反应的速率比碳酸钠快.
(2)通过查阅资料得知,小苏打受热后分解的严产物之一是Na2CO3,于是该小组的同学认为小苏打受热分解后的产物为Na2CO3和水.试分析该结论是否成立,并说明理由.不成立,不满足质量守恒定律
(3)同澄清石灰水中通入过量CO2,先生成白色沉淀,一段时间后白色沉淀又消失.原因是碳酸钙和水,CO2反应生成可溶于水的碳酸氢钙[Ca(CO3)2],写出该反应的化学方程式CaCO3+H2O+CO2=Ca(HCO3)2,该反应的基本反应类型属于化合反应.
结合已学知识,回答下列问题.
| 序号 | 实验装置 | 现象 |
| 1 | 取等质量、干燥的小苏打和纯碱,放入试管中并在酒精灯火焰上加热. | 小苏打:试管内壁有水珠,固体质量减轻; |
| 纯碱:无明显现象,固体质量不减轻. | ||
| 2 | 取等质量的小苏打和纯碱,放入试管中,再加入足量等浓度的盐酸. | 小苏打:粉末很快消失,有大量气泡冒出; |
| 纯碱:粉末很快消失,有大量气泡冒出. |
(2)通过查阅资料得知,小苏打受热后分解的严产物之一是Na2CO3,于是该小组的同学认为小苏打受热分解后的产物为Na2CO3和水.试分析该结论是否成立,并说明理由.不成立,不满足质量守恒定律
(3)同澄清石灰水中通入过量CO2,先生成白色沉淀,一段时间后白色沉淀又消失.原因是碳酸钙和水,CO2反应生成可溶于水的碳酸氢钙[Ca(CO3)2],写出该反应的化学方程式CaCO3+H2O+CO2=Ca(HCO3)2,该反应的基本反应类型属于化合反应.
6.清明时节,同学们相约外出踏青野炊.请用化学知识分析小丽问题:
(1)野炊食谱人表所示:
从合理膳食角度来看,你认为食谱中还应添加C(填字母);
A.炒鸡蛋 B.牛奶 C.黄瓜 D.烤野兔肉
(2)野炊后同学们准备将垃圾分类处理,其中属于不可回收垃圾的是B(填字母);
A.废纸 B.果皮 C.易拉罐 D.塑料桶.
(1)野炊食谱人表所示:
| 主食 | 馒头 |
| 配菜 | 红烧肉、豆腐汤、牛肉干 |
A.炒鸡蛋 B.牛奶 C.黄瓜 D.烤野兔肉
(2)野炊后同学们准备将垃圾分类处理,其中属于不可回收垃圾的是B(填字母);
A.废纸 B.果皮 C.易拉罐 D.塑料桶.
16.含有铵根离子的物质称为农业生产中的铵态氮肥,下表是氮肥氯化铵在不同温度下的溶解度:
(1)从表可知,在70℃时,50克水中最多可以溶解氯化铵30.1克.
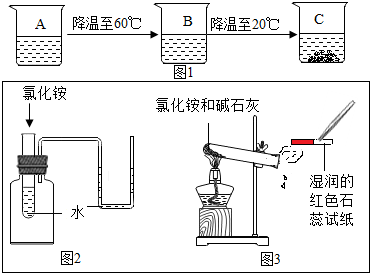
(2)烧杯A是70℃时,含有100g水的氯化铵不饱和溶液,经过如图1的变化过程(在整个过程中,不考虑水分的蒸发),则到C烧杯时溶液的质量为137.2g.
(3)如图所示,是对氯化铵性质的探究实验:
①图2说明氯化铵溶于水会吸收热量.
②图3观察到湿润的红色石蕊试纸变蓝色.
③在农业生产中不能(填“能”或“不能”)将铵态氮肥与碱性物质混用.
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| 溶解度(g) | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.0 | 60.2 |
(2)烧杯A是70℃时,含有100g水的氯化铵不饱和溶液,经过如图1的变化过程(在整个过程中,不考虑水分的蒸发),则到C烧杯时溶液的质量为137.2g.
(3)如图所示,是对氯化铵性质的探究实验:
①图2说明氯化铵溶于水会吸收热量.
②图3观察到湿润的红色石蕊试纸变蓝色.
③在农业生产中不能(填“能”或“不能”)将铵态氮肥与碱性物质混用.

3.厨房中有一瓶白色固体,小明认为它可能是食盐,小刚认为它可能是白糖,就两个人的看法而言,应属于科学探究环节中的( )
| A. | 猜想与假设 | B. | 设计实验 | C. | 获得结论 | D. | 收集证据 |
20.小平故居果山村盛产枇杷,有“枇杷之乡”之美誉.下表是100g这种枇杷的部分营养成分,请据表回答:
(1)表中的钙、钾、磷是指C;
A.分子 B.原子 C.元素 D.单质
(2)表中出现了六大营养素中的4类,其中属于维持生命活动所需能量的主要营养素是糖类;
(3)人体若缺钙,则易患B.
A.贫血病 B.佝偻病 C.甲状腺疾病 D.侏儒症.
| 营养成分 | 糖类 | 脂肪 | 蛋白质 | 钙 | 钾 | 磷 |
| 质量 | 9.3g | 0.2g | 0.8g | 17mg | 122mg | 8mg |
A.分子 B.原子 C.元素 D.单质
(2)表中出现了六大营养素中的4类,其中属于维持生命活动所需能量的主要营养素是糖类;
(3)人体若缺钙,则易患B.
A.贫血病 B.佝偻病 C.甲状腺疾病 D.侏儒症.
1.规范的实验操作是实验成功的保证.下列实验操作错误的是( )
| A. | 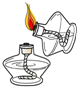 | B. | 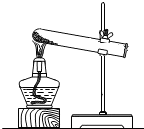 | C. | 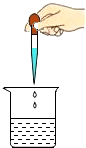 | D. |  |