题目内容
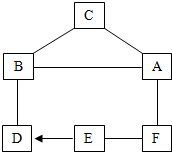 现有A~F六种物质,已知A、B、C是常见的酸、碱、盐,B常用于改良酸性土壤,A的浓溶液稀释时会释放出大量的热,E、F为常见的单质,F元素在地壳中的含量仅次于铝,D是造成温室效应的主要气体(图中“-”表示两端的物质在一定条件下能发生化学反应,“→”表示两种物质存在转化关系).
现有A~F六种物质,已知A、B、C是常见的酸、碱、盐,B常用于改良酸性土壤,A的浓溶液稀释时会释放出大量的热,E、F为常见的单质,F元素在地壳中的含量仅次于铝,D是造成温室效应的主要气体(图中“-”表示两端的物质在一定条件下能发生化学反应,“→”表示两种物质存在转化关系).(1)写出A的一种用途:
(2)E、F中由原子构成的是
(3)图中发生置换反应的化学方程式:
(4)图中发生中和反应的化学方程式:
考点:物质的鉴别、推断,化学式的书写及意义,书写化学方程式、文字表达式、电离方程式
专题:框图型推断题
分析:根据A、B、C是常见的酸、碱、盐,B常用于改良酸性土壤,所以B是氢氧化钙,A的浓溶液稀释时会释放出大量的热,所以A是硫酸,E、F为常见的单质,F元素在地壳中的含量仅次于铝,所以F是铁,D是造成温室效应的主要气体,所以D是二氧化碳,铁和单质E会反应,E又会转化成二氧化碳,所以E是氧气,盐C和硫酸、氢氧化钙都会反应,所以C是可溶性的碳酸盐,可以是碳酸钠、碳酸钾等,然后将推出的各种物质代入转化关系中验证即可.
解答:解:(1)A、B、C是常见的酸、碱、盐,B常用于改良酸性土壤,所以B是氢氧化钙,A的浓溶液稀释时会释放出大量的热,所以A是硫酸,E、F为常见的单质,F元素在地壳中的含量仅次于铝,所以F是铁,D是造成温室效应的主要气体,所以D是二氧化碳,铁和单质E会反应,E又会转化成二氧化碳,所以E是氧气,盐C和硫酸、氢氧化钙都会反应,所以C是可溶性的碳酸盐,可以是碳酸钠、碳酸钾等,C碳酸钠和A硫酸反应会生成硫酸钠、水和二氧化碳,C碳酸钠和B氢氧化钙反应会生成白色的碳酸钙沉淀和氢氧化钠,硫酸和F铁会生成硫酸亚铁和氢气,氢氧化钙和D二氧化碳会生成碳酸钙沉淀和水,F铁和E氧气会生成四氧化三铁,氧气和木炭会生成二氧化碳,推出的各种物质均满足题意,推导合理,所以A是硫酸,可以和金属氧化物反应生成盐和水,所以A的用途有:除锈,D的化学式是:CO2;
(2)通过推导可知E是氧气,F是铁,氧气是由氧气分子构成的,铁是由铁原子构成的,所以E、F中由原子构成的是:F;
(3)置换反应是单质和化合物反应生成另一种单质和另一种化合物的反应,通过分析题中的反应可知铁和硫酸反应生成硫酸亚铁和氢气,满足置换反应的定义,所以化学方程式为:Fe+H2SO4═FeSO4+H2↑;
(4)酸和碱相互交换成分生成盐和水的反应叫中和反应,通过分析题中的反应可知硫酸和氢氧化钙反应生成硫酸钙和水,满足中和反应的定义,所以化学方程式为:Ca(OH)2+H2SO4═CaSO4+2H2O.
故答案为:(1)除锈,CO2;
(2)F;
(3)Fe+H2SO4═FeSO4+H2↑;
(4)Ca(OH)2+H2SO4═CaSO4+2H2O.
(2)通过推导可知E是氧气,F是铁,氧气是由氧气分子构成的,铁是由铁原子构成的,所以E、F中由原子构成的是:F;
(3)置换反应是单质和化合物反应生成另一种单质和另一种化合物的反应,通过分析题中的反应可知铁和硫酸反应生成硫酸亚铁和氢气,满足置换反应的定义,所以化学方程式为:Fe+H2SO4═FeSO4+H2↑;
(4)酸和碱相互交换成分生成盐和水的反应叫中和反应,通过分析题中的反应可知硫酸和氢氧化钙反应生成硫酸钙和水,满足中和反应的定义,所以化学方程式为:Ca(OH)2+H2SO4═CaSO4+2H2O.
故答案为:(1)除锈,CO2;
(2)F;
(3)Fe+H2SO4═FeSO4+H2↑;
(4)Ca(OH)2+H2SO4═CaSO4+2H2O.
点评:在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目
下列物质久置在空气中发生的变化,属于物理变化的是( )
| A、氢氧化钠质量增加 |
| B、浓硫酸质量增加 |
| C、生石灰质量增加 |
| D、铁钉生锈质量增加 |
下列说法不正确的是( )
| A、长期饮用硬水对人体的健康不利 |
| B、用洗洁精清洗餐具上的油污是乳化作用 |
| C、用氢氧化钠治疗胃酸过多 |
| D、空气中灼烧铜片后质量增加符合质量守恒定律 |
下列生活中的现象,属于化学变化的是( )
| A、榨取果汁 | B、铁锅生锈 |
| C、湿衣服晾干 | D、水制冰块 |