题目内容
15. 实验室中有一瓶标签受损的无色液体,如图所示,这瓶无色液体是什么呢?王老师告诉大家,该液体是碳酸钠溶液、氢氧化钠溶液中的一种.
实验室中有一瓶标签受损的无色液体,如图所示,这瓶无色液体是什么呢?王老师告诉大家,该液体是碳酸钠溶液、氢氧化钠溶液中的一种.【猜想】①该溶液是氢氧化钠溶液;②该溶液为碳酸钠溶液
【资料】氢氧化钡是能溶于水的白色固体,碳酸钡是不溶于水的白色固体.
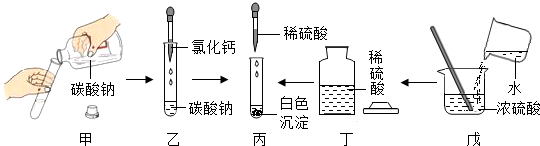
【设计与实验】三位同学个设计了一个方案,并根据各自方案实验,记录如下:
| 实验操作 | 实验现象 | 结论 | |
| A | 取样于试管中,滴加数滴稀盐酸 | 无明显现象 | 溶质只有氢氧化钠 |
| B | 向试管中加入一定质量的稀盐酸,再滴加几滴样品 | 有气体产生 | 溶质只有碳酸钠 |
| C | 取样于试管中,滴加数滴氯化钡溶液 | 出现白色沉淀 | 溶液中含有碳酸钠 |
(1)A、B两位同学所用试剂相同,但现象与结论不同,其原因是氢氧化钠与碳酸钠的混合物溶液与盐酸反应,只有氢氧化钠完全反应后,才能观察到有气体产生,是否产生气体与盐酸用量有关
(2)分析三位同学的实验,一致认为该溶液中溶质为氢氧化钠和碳酸钠.请你另设计一个实验证明溶液中的溶质既有碳酸钠,又有氢氧化钠(写出操作与现象):取试样与试管中,加入足量的氯化钡溶液,直至没有沉淀产生,然后向上层清液中加入酚酞试液,溶液变红.
【反思】造成这瓶试剂中出现两种溶质的原因用化学方程式表示为2NaOH+CO2═Na2CO3+H2O.
分析 氢氧化钠能与二氧化碳反应生成碳酸钠和水,根据氢氧化钠、碳酸钠的水溶液显碱性,碳酸钠能与氯化钡溶液反应生成碳酸钡白色沉淀,进行分析解答.
解答 解:若是只有氢氧化钠,则加入盐酸没有明显的现象,若是只有碳酸钠,则加入盐酸即有气泡产生,故填:
| 实验操作 | 实验现象 | 结论 | |
| A | 取样于试管中,滴加数滴稀盐酸 | 无明显现象 | 溶质只有氢氧化钠 |
| B | 向试管中加入一定质量的稀盐酸,再滴加几滴样品 | 有气体产生 | 溶质只有碳酸钠 |
| C | 取样于试管中,滴加数滴氯化钡溶液 | 出现白色沉淀 | 溶液中含有碳酸钠 |
(2)要证明氢氧化钠和碳酸钠同时存在,则需要加入氯化钡溶液除去碳酸钠,再加入酚酞试液根据变红证明含有氢氧化钠,故填:取试样与试管中,加入足量的氯化钡溶液,直至没有沉淀产生,然后向上层清液中加入酚酞试液,溶液变红;
(3)氢氧化钠能与二氧化碳反应生成碳酸钠和水,故填:2NaOH+CO2═Na2CO3+H2O.
点评 本题考查的是常见变质药品成分的实验探究,完成此题,可以依据已有的知识进行.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案
相关题目
3.实验室需要100g质量分数3%氯化钠溶液,配制过程中相关描述正确的是( )
| A. | 氯化钠直接放于天平托盘上称取 | |
| B. | 直接用手抓取氯化钠 | |
| C. | 用3g氯化钠与100g水配制得到 | |
| D. | 用50g质量分数6%氯化钠溶液与50g水配制得到 |
17.下列变化一定属于化学变化的是( )
| A. | 打开弄盐酸瓶盖,从瓶口涌出白雾 | |
| B. | 打磨过的光亮铝条置于空气中表面逐渐变暗 | |
| C. | 固体碘受热后变成紫红色碘蒸汽 | |
| D. | 氧气通过低温加压变成了淡蓝色液体 |
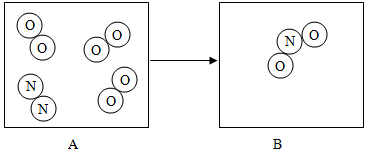

 液化气是生活中常用燃料,如图是液化气燃气灶具的示意图.
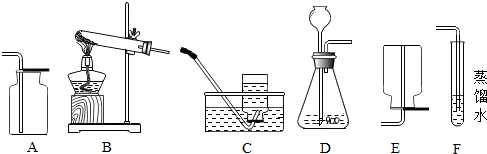
液化气是生活中常用燃料,如图是液化气燃气灶具的示意图. 如图为制取氢气的装置图,实验时先打开弹簧夹,再打开分液漏斗活塞a.
如图为制取氢气的装置图,实验时先打开弹簧夹,再打开分液漏斗活塞a.