题目内容
5.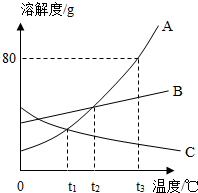 如图所示,依据A、B、C三种物质的溶解度曲线,回答下列问题
如图所示,依据A、B、C三种物质的溶解度曲线,回答下列问题(1)t2℃时,A、B、C三种物质的溶解度的关系是A=B>C(用“>”、“<”或“=”表示).
(2)t2℃时,A、B、C三种物质的饱和溶液各100g,分别降温到t1℃时,所得溶液质量的关系是C>B>A (用“>”、<”或“=”表示).
(3)t3℃时,A物质饱和溶液中,溶质、溶剂、溶液的质量之比为4:5:9 (填最简比).
(4)t3℃时,将等质量的A、B两种物质加水溶解配制成饱和溶液,所需水的质量较多的是B.
(5)A中含有少量的B,若要提纯A,可采用降温结晶的方法.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)通过分析溶解度曲线可知,t2℃时,A、B、C三种物质的溶解度的关系是A=B>C;
(2)t2℃时,A、B、C三种物质的饱和溶液各100g,分别降温到t1℃时,A物质的溶解度不会最大,B物质次之,C物质不会析出晶体,所以所得溶液质量的关系是C>B>A;
(3)t3℃时,A物质的溶解度是80g,所以A物质饱和溶液中,溶质、溶剂、溶液的质量之比为80g:100g:180g=4:5:9;
(4)t3℃时,B物质的溶解度小于A物质,所以将等质量的A、B两种物质加水溶解配制成饱和溶液,所需水的质量较多的是B;
(5)A物质的溶解度受温度变化影响较大,所以A中含有少量的B,若要提纯A,可采用降温结晶的方法.
故答案为:(1)A=B>C;
(2)C>B>A;
(3)t3℃时,A物质的溶解度是80g,所以A物质饱和溶液中,溶质、溶剂、溶液的质量之比为80g:100g:180g=4:5:9;
(4)B;
(5)降温结晶.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.如图实验操作不正确的是( )
| A. |  | B. |  | C. |  | D. |  |
20.除去如表物质中的少量杂质,所选用试剂及方法均正确的是( )
| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | CO2(CO) | 过量O2 | 点燃 |
| B | CaO(Ca C03) | 足量蒸馏水 | 过滤、蒸发 |
| C | NaCl溶液(Mg SO4) | 适量BaCl2 | 过滤 |
| D | FeCl2溶液(CuCl2溶液) | 足量铁粉 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
10.在铁与稀硫酸的反应中,化合价在化学反应前后发生变化的元素是( )
| A. | 氢和氧 | B. | 铁和氢 | C. | 铁和硫 | D. | 氧和硫 |
17.将一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如表:
下列说法错误的是( )
| 物质 | a | b | c | d |
| 反应前质量(g) | 6.4 | 3.2 | 4.0 | 0.5 |
| 反应后质量(g) | 待测 | 2.56 | 7.2 | 0.5 |
| A. | 该反应是化合反应 | |
| B. | a的待测值为3.84g | |
| C. | a和b是反应物,d是催化剂 | |
| D. | 若a与b的相对分子质量之比为2:1,则反应中a与b的化学计量数之比为2:1 |
14.下列各组物质的稀溶液,不用其它试剂就能鉴别出来的是( )
| A. | FeCl3、NaOH、Na2SO4、KCl | B. | Na2CO3、HCl、CaCl2、BaCl2 | ||
| C. | NH4Cl、KOH、Na2SO4、BaCl2 | D. | KNO3、HCl、NaOH、CuCl2 |
15.用Mg、MgO、Mg(OH)2、MgCO3、HCl五种物质两两进行反应,能得到MgCl2 的方法有( )
| A. | 3种 | B. | 4种 | C. | 2种 | D. | 无法确定 |
 2015年3月18日,中科院院土谢毅教授凭借发现二维超薄半导体在提高光电、热电转换效率方面的工作,获得第17届“世界杰出女科学家成就奖”.Ca2S3 (硫化镓)是制作二维超薄半导体的材料之一.图I、图II分别是硫元素和镓元素在元素周期表中的信息,图III分别是硫原子的原子结构示意图.
2015年3月18日,中科院院土谢毅教授凭借发现二维超薄半导体在提高光电、热电转换效率方面的工作,获得第17届“世界杰出女科学家成就奖”.Ca2S3 (硫化镓)是制作二维超薄半导体的材料之一.图I、图II分别是硫元素和镓元素在元素周期表中的信息,图III分别是硫原子的原子结构示意图.