题目内容
7.黄铜渣中约含Zn 7%、ZnO 31%、Cu 50%、CuO 5%,其余为杂质.处理黄铜渣可得到硫酸锌,其主要流程如下图(杂质不溶于水、不参与反应):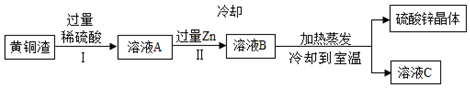
下列说法正确的是( )
| A. | 溶液A中的溶质有2种 | B. | Ⅰ、Ⅱ中的操作均包含过滤 | ||
| C. | 溶液A的质量大于溶液B | D. | 溶液C中溶质的质量分数小于溶液B |
分析 稀硫酸和锌反应生成硫酸锌和氢气,和氧化锌反应生成硫酸锌和水,和氧化铜反应生成硫酸铜和水,不能和铜反应;
锌和硫酸铜反应生成硫酸锌和铜.
解答 解:A、溶液A中的溶质有硫酸锌、硫酸铜和硫酸3种,该选项说法不正确;
B、Ⅰ、Ⅱ中的操作均包含过滤,通过过滤把液体和固体分离,该选项说法正确;
C、溶液A转化到溶液B的过程中,锌和硫酸铜反应生成硫酸锌和铜,和硫酸反应生成硫酸锌和氢气,反应的化学方程式及其质量关系为:
Zn+CuSO4═ZnSO4+Cu,Zn+H2SO4═ZnSO4+H2↑,
65 64 65 2
由以上质量关系可知,随着反应进行,溶液质量增大,因此溶液A的质量小于溶液B的质量,该选项说法不正确;
D、溶液C中是硫酸锌的饱和溶液,溶液B中是硫酸锌的饱和溶液或不饱和溶液,温度相同,都是室温,因此溶液C中溶质的质量分数大于或等于溶液B,该选项说法不正确.
故选:B.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.2014年2月11日广州署潮州市公安机关,查处12吨博大食品生产的含三聚氰胺的酸奶片.三聚氰胺的化学式C3H6N6,下列关于三聚氰胺的说法正确的是( )
| A. | 三聚氰胺是由3个碳原子、6个氢原子、6个氮原子组成 | |
| B. | 三聚氰胺的相对分子质量为126g | |
| C. | 三聚氰胺中碳、氢、氮元素的质量比为1:2:2 | |
| D. | 三聚氰胺中氮元素质量分数为66.7% |
15.下列实验操作中,正确的是( )
| A. | 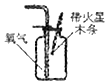 氧气的验满 | B. | 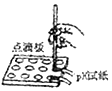 测溶液的酸碱度 | C. | 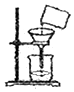 分离固液混合物 | D. | 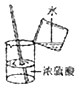 稀释浓硫酸 |
16.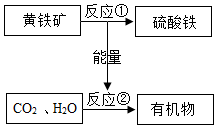 “细菌冶金”的原理是利用氧化铁硫杆菌促使 黄铁矿(主要成分FeS2)氧化成硫酸铁和硫酸,并能为CO2和H2O合成有机物提供能量.流程如图,下列说法错误的是( )
“细菌冶金”的原理是利用氧化铁硫杆菌促使 黄铁矿(主要成分FeS2)氧化成硫酸铁和硫酸,并能为CO2和H2O合成有机物提供能量.流程如图,下列说法错误的是( )
 “细菌冶金”的原理是利用氧化铁硫杆菌促使 黄铁矿(主要成分FeS2)氧化成硫酸铁和硫酸,并能为CO2和H2O合成有机物提供能量.流程如图,下列说法错误的是( )
“细菌冶金”的原理是利用氧化铁硫杆菌促使 黄铁矿(主要成分FeS2)氧化成硫酸铁和硫酸,并能为CO2和H2O合成有机物提供能量.流程如图,下列说法错误的是( )| A. | 反应①化学方程式:4FeS2+15O2+2X=2Fe2(SO4)3+2H2SO4,X为H2O2 | |
| B. | 整个流程提高了能量的利用率 | |
| C. | 图中有机物一定不含氧元素 | |
| D. | 氧化铁硫杆菌在反应①中起催化作用 |
8.下列知识归纳中,完全正确的是( )
| A.化学常识 | B.化学与生活 |
| ①活性炭除异味是利用它的吸附性 ②铵态氮肥不能与碱性物质混合使用 ③充入氮气食品防腐 | ①用pH试纸测定洗发水的酸碱度 ②用氢氧化钠改良酸性土壤 ③碳酸氢钠是焙制糕点发酵粉成分之一 |
| C.化学与健康 | D.化学与安全 |
| ①人体缺维生素C易患坏血病 ②海鲜防腐可以用甲醛溶液浸泡 ③霉变的大米可高温加热后食用 | ①图书、档案着火,用CO2灭火器灭火 ②在室内放一盆水,可防止煤气中毒 ③为防止矿井中瓦斯爆炸,严禁吸烟 |
| A. | A | B. | B | C. | C | D. | D |
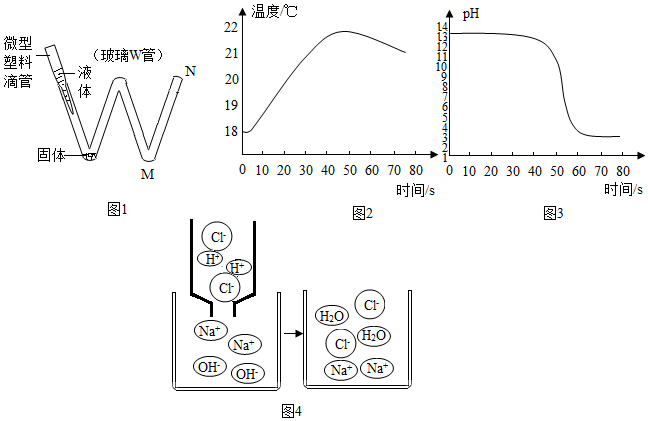
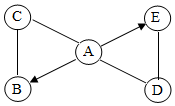 A、B、C、D、E为初中化学常见的五种物质,它们之间有如图所示的转化和反应关系(“→”表示某一种物质经一步反应可转化为另一种物质,“-”表示相连物质能发生化学反应,部分反应物、生成物及反应条件已略去).
A、B、C、D、E为初中化学常见的五种物质,它们之间有如图所示的转化和反应关系(“→”表示某一种物质经一步反应可转化为另一种物质,“-”表示相连物质能发生化学反应,部分反应物、生成物及反应条件已略去).