题目内容
5.分析推理是一种重要的化学思维方法.下列推理正确的是( )| A. | 分子、原子可以构成物质,所以物质一定是由分子、原子构成的 | |
| B. | 碱性溶液能使酚酞试液变红色,所以能使酚酞试液变红色的溶液的pH一定大于7 | |
| C. | 溶液的特征是均一、稳定,所以均一、稳定的液体一定是溶液 | |
| D. | 稀有气体元素的原子最外层有8个(氦是2个)电子,所以微粒 一定是稀有气体元素的原子 一定是稀有气体元素的原子 |
分析 A、根据构成物质的微粒有分子、原子和离子解答;
B、根据碱性溶液能使酚酞试液变红色,pH大于7解答;
C、根据均一、稳定的液体不一定是溶液考虑;
D、根据原子最外层电子数为8(氦除外)的微粒可能一原子阳离子或阴离子解答.
解答 解:
A、分子、原子可以构成物质,所以物质不一定是由分子、原子构成的,构成物质的微粒有分子、原子和离子,可能是离子构成,故错误;
B、碱性溶液能使酚酞试液变红色,因此能使酚酞试液变红色的溶液的pH一定大于7,故正确;
C、溶液的特征是均一、稳定,但均一、稳定的液体不一定是溶液,例如水,故错误;
D、原子最外层电子数为8(氦除外)的微粒可能是原子、阳离子或阴离子,因此微粒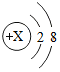 不一定是稀有气体元素的原子,故错误.
不一定是稀有气体元素的原子,故错误.
答案:B
点评 本题难度较大,此题说明物质不同,性质不同,不能用类推法来学习化学,要熟记相关基础知识是正确解题的关键.

练习册系列答案
相关题目
20.水是生命之源.下列有关水的说法正确的是( )
| A. | 长期饮用蒸馏水有利于人体健康 | |
| B. | 水的天然循环是通过其三态变化实现的 | |
| C. | 活性炭能使河水转化为纯净水 | |
| D. | 电解水时正极产生的气体可作新型燃料 |
4.质量守恒定律是一切化学变化都必须遵循的一个重要定律,对于我们对化学变化的定性研究和定量研究都有着极其重要的指导作用.
(1)定性研究:在实验室中,不能用带磨口玻璃塞的玻璃试剂瓶盛装氢氧化钠溶液,因为氢氧化钠会与玻璃成分中的某种物质X发生化学反应,使玻璃塞和玻璃试剂瓶口粘连在一起.其反应的化学方程式为X+2NaOH═Na2SiO3+H2O,则X的化学式为SiO2.
(2)定量研究:酒精是乙醇的俗称,可用于医疗消毒,也常作燃料.在氧气充足的条件下完全燃烧的生成物为二氧化碳和水,现将一定质量的乙醇和氧气放在密闭容器中,它们恰好完全燃烧,测得反应前后各物质的质量如表所示.请答题:
①根据质量守恒定律可知,a=9.6;
②生成物中,二氧化碳中碳元素的质量为2.4g,水中氢元素的质量为0.6g;
③由于氧气只含氧元素,故生成物中的碳元素和氢元素都来自于反应物中的乙醇,结合上面的计算结果可知,乙醇中一定含有(选填“含有”或“不含有”)氧元素,其质量为1.6g,乙醇所含碳、氢、氧元素的质量比为12:3:8,原子个数比为2:6:1.
(1)定性研究:在实验室中,不能用带磨口玻璃塞的玻璃试剂瓶盛装氢氧化钠溶液,因为氢氧化钠会与玻璃成分中的某种物质X发生化学反应,使玻璃塞和玻璃试剂瓶口粘连在一起.其反应的化学方程式为X+2NaOH═Na2SiO3+H2O,则X的化学式为SiO2.
(2)定量研究:酒精是乙醇的俗称,可用于医疗消毒,也常作燃料.在氧气充足的条件下完全燃烧的生成物为二氧化碳和水,现将一定质量的乙醇和氧气放在密闭容器中,它们恰好完全燃烧,测得反应前后各物质的质量如表所示.请答题:
| 物质质量 | 乙醇 | 氧气 | 二氧化碳 | 水 |
| 反应前/g | 4.6 | a | 0 | 0 |
| 反应后/g | 0 | 0 | 8.8 | 5.4 |
②生成物中,二氧化碳中碳元素的质量为2.4g,水中氢元素的质量为0.6g;
③由于氧气只含氧元素,故生成物中的碳元素和氢元素都来自于反应物中的乙醇,结合上面的计算结果可知,乙醇中一定含有(选填“含有”或“不含有”)氧元素,其质量为1.6g,乙醇所含碳、氢、氧元素的质量比为12:3:8,原子个数比为2:6:1.
2.如表是NaCl和KNO3在不同温度时的溶解度,回答问题
(1)两种物质中,溶解度受温度影响变化较大的是KNO3.
(2)60℃时,按图示操作:

A中溶液是不饱和(填“饱和”或“不饱和”)溶液,C中溶液的总质量是167.6g.
(3)50℃时,将两种物质的饱和溶液各100g,分别加热蒸发10g水后,再恢复到50℃,剩余溶液的质量:NaCl溶液大于(填“大于”“等于”或“小于”)KNO3溶液.
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 | |
(2)60℃时,按图示操作:

A中溶液是不饱和(填“饱和”或“不饱和”)溶液,C中溶液的总质量是167.6g.
(3)50℃时,将两种物质的饱和溶液各100g,分别加热蒸发10g水后,再恢复到50℃,剩余溶液的质量:NaCl溶液大于(填“大于”“等于”或“小于”)KNO3溶液.
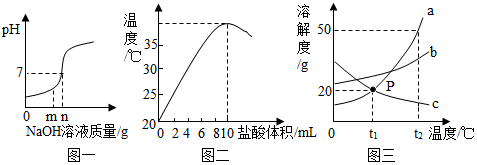
 如图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题:
如图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题: