题目内容
配制100g 8%的硫酸铜溶液,步骤如下:(1)计算:需要硫酸铜______g,水______mL.
(2)称量:用托盘天平称取硫酸铜固体,放入烧杯中,用规格为______量筒(填“10mL”或“100mL”)量取水,也倒入烧杯中.
(3)溶解:用玻璃棒搅拌溶解.
【答案】分析:利用溶质的质量等于溶液质量与溶质质量分数的乘积,再结合溶液质量是溶质与溶剂质量之和解决.
解答:解:(1)溶液质量与溶质质量分数的乘积是溶质的质量,则有100g×8%=8g因为溶液的质量等于溶质与溶剂的质量之和,则有水的质量=100g-8g=92g,根据密度公式可知水的体积为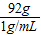 =92ml
=92ml
(2)量取92mL的水需用100mL的量筒;
故答案为:(1)8 92 (2)100 mL
点评:此题是对溶液知识的考查题,解题的关键是掌握溶质质量的求法,是基本的溶液计算题.
解答:解:(1)溶液质量与溶质质量分数的乘积是溶质的质量,则有100g×8%=8g因为溶液的质量等于溶质与溶剂的质量之和,则有水的质量=100g-8g=92g,根据密度公式可知水的体积为
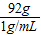 =92ml
=92ml(2)量取92mL的水需用100mL的量筒;
故答案为:(1)8 92 (2)100 mL
点评:此题是对溶液知识的考查题,解题的关键是掌握溶质质量的求法,是基本的溶液计算题.

练习册系列答案
相关题目