题目内容
15.最早提出原子论和分子学说的科学家是道尔顿和阿伏加德罗,奠定了近代化学基础.其主要内容是物质是由分子和原子构成的,分子的破裂和原子的重组是化学变化的基础.俄国科学家门捷列夫是最早发现和提出了元素周期律 和元素周期表.分析 根据科学家们各自在科学上做出的贡献,进行分析解答本题.
解答 解:道尔顿在化学上的主要贡献是提出了原子学说,阿伏加德罗在化学上的主要贡献是提出了分子的概念,并创立了分子学说,最早提出原子论和分子学说的科学家是道尔顿和阿伏加德罗,奠定了近代化学基础.其主要内容是物质是由分子和原子构成的,分子的破裂和原子的重组是化学变化的基础.
俄国科学家门捷列夫是最早发现和提出了元素周期律,并编制出元素周期表.
故答案为:道尔顿;阿伏加德罗;物质是由分子和原子构成的;分子的破裂和原子的重组是化学变化的基础;元素周期律;元素周期表.
点评 本题难度不大,了解化学的发展历史,关注化学学科成就,有利于激发学生学习化学的兴趣,培养学生的社会责任感.

练习册系列答案
相关题目
6.在 C3N4中,N的化合价为-3?则C的化合价是( )
| A. | -4 | B. | -3 | C. | +4 | D. | +3 |
3.1777年舍勒在《火与空气》一书中指出:空气由两种性质不同的“火空气”和“浊空气”组成,其中“火空气”可以帮助燃烧,维持生命.下列物质不能与“火空气”发生化学反应的是( )
| A. | 木炭 | B. | 酒精 | C. | 蒸馏水 | D. | 铁丝 |
20.小睿从课外资料中得知葡萄糖(C6H12O6)具有可燃性,于是他和小组同学展开探究:
提出问题】葡萄糖在氧气中燃烧可能生成什么?
【猜想与假设】可能会生成二氧化碳、水、一氧化碳和二氧化硫中的一种或几种
讨论与交流】小军认为不可能生成二氧化硫,其理由是葡萄糖中不含有硫元素.
【查阅资料】无水硫酸铜遇水变蓝色;CO能与PdCl2溶液生成黑色的金属Pd.
【实验探究】同学们设计了如下装置来探究
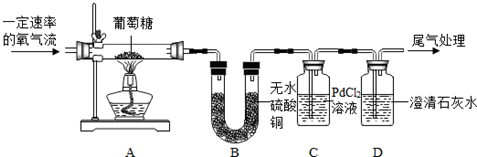
【反思与交流】装置B和装置C的顺序能否颠倒?不能,(填“能”或“不能”)理由理由
理由颠倒后不能判断是否有水生成了.
提出问题】葡萄糖在氧气中燃烧可能生成什么?
【猜想与假设】可能会生成二氧化碳、水、一氧化碳和二氧化硫中的一种或几种
讨论与交流】小军认为不可能生成二氧化硫,其理由是葡萄糖中不含有硫元素.
【查阅资料】无水硫酸铜遇水变蓝色;CO能与PdCl2溶液生成黑色的金属Pd.
【实验探究】同学们设计了如下装置来探究

| 现象 | 结论或化学方程式 |
| 装置B中的无水硫酸铜变蓝色 | 它燃烧生成了水 |
| PdCl2溶液中出现了黑色的金属 | 它燃烧生成了CO |
| 装置D中的澄清石灰水变浑浊 | 它燃烧生成了CO2,装置D中发生反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O. |
理由颠倒后不能判断是否有水生成了.
20.下列符号既可以表示一种元素又可以表示这种元素的一个原子还可以表示这种物质的是( )
| A. | H | B. | F | C. | N | D. | S |
1.鉴别下列各组物质,括号中选用的试剂或方法,不合理的是( )
| A. | 酒精和氯化钠溶液(闻气味) | |
| B. | 氢氧化钠溶液和稀硫酸(酚酞试液) | |
| C. | 澄清的石灰水和氢氧化钠溶液(稀盐酸) | |
| D. | 硫酸铜溶液和硫酸亚铁溶液(观察颜色) |
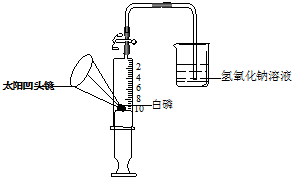 如下是小晶同学对“久未开启的菜窖内气体成分”的探究过程:
如下是小晶同学对“久未开启的菜窖内气体成分”的探究过程: